Esperion公司日前宣布,其降低低密度脂蛋白胆固醇(LDL-C)的在研药物bempedoic acid已完成共包含五项3期临床试验整个3期临床研发项目,累积结果证明了bempedoic acid单药使用以及与ezetimibe联合使用的良好疗效、安全性与耐药性,有望治疗包括动脉粥样硬化心血管疾病(ASCVD)和/或杂合子家族性高胆固醇血症(HeFH)在内的心血管病高风险患者。

高水平的LDL-C可导致动脉内壁的脂肪及胆固醇积聚,即动脉粥样硬化。动脉粥样硬化可导致包括心脏病或中风在内的心血管事件。在美国,约7800万人(超过全国人口的20%)有较高的LDL-C水平,而欧洲和日本分别为7300万和3000万人。其中,美国约有1300万ASCVD患者,他们即便使用最大耐受剂量的他汀类药物疗法,仍然无法使LDL-C水平得到控制。除此之外,一些患者还具有他汀类药物不耐受,这也导致患者们具有高心血管病风险。超过600万的ASCVD和/或HeFH患者在接受最大耐受他汀类药物治疗后仍需要额外降低近30%的LDL-C水平来实现治疗目标。因此,患者们急需一款新的治疗选择来帮助他们降低LDL-C水平。
Esperion公司的bempedoic acid是一款口服,创新ATP柠檬酸裂解酶(ACL)抑制剂。它通过降低胆固醇的生物合成,和调控LDL受体来降低LDL-C水平。该药可以对现有口服疗法进行补充,帮助患者们额外降低LDL-C水平。与他汀类药物相似,bempedoic acid也可以降低高敏C反应蛋白(hsCRP),一个与心血管疾病相关的炎症的关键标志物。Bempedoic acid可与ezetimibe联用,ezetimibe可以抑制NPC1L1(Niemann-Pick C1-Like 1),降低胃肠道内胆固醇的吸收,从而降低胆固醇对肝脏的输送。
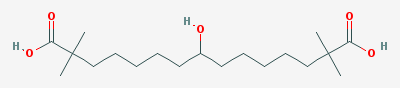
▲Bempedoic acid分子结构(图片来源:PubChem)
Esperion于2016年1月开始进行全球范围的关键3期临床发展项目,旨在评估bempedoic acid单用以及与ezetimibe联用的安全性、耐药性以及作为补充疗法持续降低LDL-C的疗效。项目包含的患者为ASCVD或有较高风险患上ASCVD的患者,这些潜在患者具有高胆固醇血症,他们在接受了最大耐受剂量他汀类药物及ezetimibe治疗后仍有较高的LDL-C水平,因此有很高的风险患上心血管疾病。项目共包含五项试验,共有约4000名患者参与,其中四项试验为bempedoic acid单药疗法关键试验(Studies 1、2、3和4),一项为bempedoic acid与ezetimibe联用疗法关键试验(053 Study)。
该3期项目的累计结果表明,bempedoic acid对比安慰剂可以将LDL-C水平额外降低18-31%(p<0.001)、在治疗意向分析中将LDL-C水平额外降低17-28%(p<0.001)、将hsCRP水平降低19-33%、以及在1002名糖尿病患者中对比安慰剂降低0.19-0.31%的血红蛋白A1c(HbA1c)。
Esperion计划于2019年第一季度向FDA提交bempedoic acid单药以及与ezetimibe联用的新药申请(NDAs),并于第二季度向EMA提交营销授权申请(MAAs)。
我们祝贺bempedoic acid的3期开发项目顺利结束,并期待该药可以早日获得批准,与患者见面。
参考资料:
[1] Esperion Announces Completion of Phase 3 LDL-C Lowering Development Program of Bempedoic Acid and Positive Cumulative Results. Retrieved October 29, 2018, from https://markets.businessinsider.com/news/stocks/esperion-announces-completion-of-phase-3-ldl-c-lowering-development-program-of-bempedoic-acid-and-positive-cumulative-results-1027662740
[2] Esperion Eyes Early 2019 to File NDA for Cholesterol-Lowering Therapy. Retrieved October 29, 2018, from https://www.biospace.com/article/esperion-eyes-early-2019-to-file-nda-for-cholesterol-lowering-therapy/
[3] LDL胆固醇水平降低35%,降脂组合疗法临床3期结果积极. Retrieved October 29, 2018, from https://mp.weixin.qq.com/s/kJkAvkBxmdTMr9qilZrL1w

