2018年11月8日,Cabaletta Bio公司公布与宾夕法尼亚大学签署独家许可协议和多年赞助研究协议。其完成3800万美元的A轮融资,将用于针对寻常性天疱疮的DSG3-CAAR-T进入临床开发。
本次融资由5AM Ventures领投,Adage Capital Management(创始投资人)和宾夕法尼亚大学参投。Adage Capital Management是美国第二大专注于医疗健康领域的股权投资公司。
正好今日,Cabaletta Bio公司技术持有人Micheal Milone教授正在受北京大学邀请参加恺思俱乐部协办的北京大学“生物技术产品新纪元——创新突破2020”国际论坛,并接受北京大学免疫系授予客座教授的荣誉称号。


CTL-019原创团队的两位主要成员Michael Milone与许中伟教授相会北京共同参加北京大学国际论坛
论坛现场我们对Michael Milone教授进行了采访。Milone教授表示,这一轮融资主要是用来进行临床试验,而且有信心让CAART技术生产成本降低,未来有计划通过IMCT国际多中心临床试验为中国的PV患者带来更好的治疗方式。另外,作为宾夕法尼亚大学的教授,他对科研更感兴趣,公司运营将交给专业的人士来做。提到癌症治疗中棘手的实体瘤,Milone教授也对CAR-T技术在这方面的应用和表现充满兴趣和期待,治疗实体瘤也是未来的癌症治疗的努力方向和机会。

恺思俱乐部访谈Michael Milone教授与许中伟教授
关于Cabaletta Bio
Cabaletta Bio是一家专注于研发B细胞介导的自身免疫病细胞疗法的生物制药公司,已经与宾夕法尼亚大学签署独家许可协议和两个多年赞助研究协议。另外,该公司还进入了宾大雇主服务协议,允许其签订科学、临床和制造专业技术协议,从而基于宾夕法尼亚大学研究团队在《科学》杂志上发表的令人信服的概念验证数据,针对寻常天疱疮(mPV)开发首个CAAR产品。
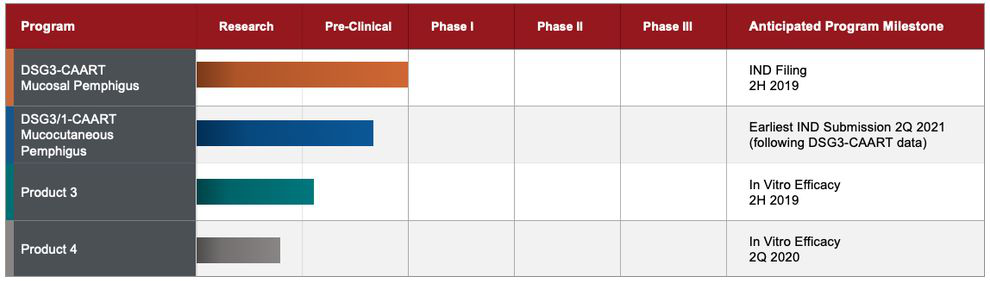
Cabaletta Bio公司管线
这种被称为寻常天疱疮(pemphigus vulgaris,PV)的自身免疫性疾病,患者的B细胞会产生抗体攻击一种名为desmoglein-3(DSG3)的蛋白,它的作用是使皮肤细胞粘附在一起。如果不治疗,PV会引发大范围的皮肤水泡,几乎是致命的。Cabaletta Bio的龙头产品就是选择性消除对DSG3产生抗体攻击的B细胞。最近Cabaletta Bio完成3800万美元的A轮融资,将用于支持针对寻常性天疱疮的DSG3-CAART进入临床开发。

Dsg-3在皮肤中的作用
“在过去的18个月中,Cabaletta推出了一系列CAAR-T细胞治疗产品,授权基础知识产权,为加速高度特异的CAAR-T细胞疗法,在细胞疗法产品研究、开发、生产和注册审批阶段汇集顶尖科学家,临床医生和专家。”Cabaletta Bio联合创始人、首席执行官兼董事长Steven Nichtberger博士说,“宾大开发了革命性嵌合抗原受体CAR-T细胞技术,并且获批用于治疗一些B细胞介导的癌症,而CAAR-T细胞对T细胞的改造也基于此。我们相信CART在B细胞介导癌症中的成功降低了CAAR-T在B细胞介导自身免疫疾病中应用的风险。因为B细胞介导的自身免疫疾病中,经常应用长期且广泛的免疫抑制疗法,然而仅有短暂的疗效和显著的副作用。”
Cabaletta由Michael Milone博士,Aimee Payne博士和Steven Nichtberger博士创立,Cabaletta的基础平台和主要资产来源于公司两位联合创始人(Michael Milone, M.D., Ph.D和Aimee Payne, M.D., Ph.D)在Penn的早期工作。
Milone博士,是病理学和检验医学副教授,自宾大细胞免疫治疗中心成立以来就是其中的成员,是CTL019(tisgenlecleucel, Kymriah®, Novartis)的共同发明人,CTL019是第一个在美国和欧洲获得监管部门批准CAR-T细胞疗法,他还一同发明了多种针对多发性骨髓瘤和实体瘤新CAR-T细胞疗法(目前处于早期临床试验)。Milone博士有超过15年的经验开发基因工程T细胞疗法,包括2004-2007年与Carl June博士的博士后奖研究。他现在带领一组转化研究人员开发用于过继性T细胞免疫治疗的新型基因工程T细胞。
Milone博士说,“我们在宾大的工作,还有其他研究者在其他机构的工作,都在临床水平证明CAR-T疗法有治疗其他严重恶性疾病的价值。通过我们的不懈努力,已经证明这个核心平台通过略微修改就可以用于针对B细胞介导的自身免疫疾病。Cabaletta的成立旨在加快这项重要工作,为患者找到新的更好的解决方案。”

DSG3-CAAR的组织学效果
Payne博士,是Albert M.Kligman皮肤病学副教授和宾夕法尼亚州Autoimmune Blistering Clinic的主任医师,致力于研究自身免疫在天疱疮和皮肤起泡B细胞介导的自身免疫性疾病是如何发生的,并为此开发新型靶向疗法。Payne博士的实验室开创了CAAR-T细胞治疗概念,用于靶向消除自身反应性B细胞,并开展了临床前概念验证工作,证明DSG3-CAAR T细胞可以在动物模型中有效控制疾病,该成果发表在Science杂志上。
“粘膜性寻常型天疱疮是一种罕见的自身免疫性疾病,会在粘膜上引起疼痛性水疱并增加严重感染的风险,”Payne博士说,“目前的治疗方法,主要是免疫抑制剂,虽很有效,但可能产生非常严重的副作用。CAAR-T细胞的高度靶向性表明可以在不影响正常B细胞功能的情况下消除致病性B细胞,这是功效和安全性的潜在理想组合。我们期待在短期内将这项项目推向临床。”
据悉,DSG3-CAART的初步临床试验活动将与宾夕法尼亚大学的合作者一起进行,宾大的合作者已经参与了二十多项新型细胞疗法和基因疗法的首次人体临床研究。用于该试验的DSG3-CAART的制造预计将由宾大的同一组织完成,该组织在过去十年中为患者制造了二十多种细胞和基因治疗方案的细胞治疗产品。
(注:Drs Milone,Payne和Nichtberger都是宾大教员,持有公司股权,宾夕法尼亚大学是公司的股权持有人和投资者。此外,宾大和许可技术的发明者将来可能会根据许可获得额外的经济利益。)
关于CAAR-T细胞疗法
嵌合自身抗体受体(CAAR)T细胞仅结合破坏致病B细胞,并不攻击对人类健康至关重要的正常B细胞。CAAR-T细胞基于宾夕法尼亚大学开发的革命性嵌合抗原受体CART细胞技术开发。CAAR-T细胞不是靶向CD19,而是在其表面上表达自身抗体靶向的抗原。4-1BB共刺激结构域和CD3-zeta信号域执行与CAR-T设置中相同的激活和细胞毒性功能。因此,Cabaletta的CAARs指挥患者的T细胞仅杀死自身反应性B细胞群,这可能完全且持久地缓解疾病,同时保留所有其他提供有益免疫的B细胞群。
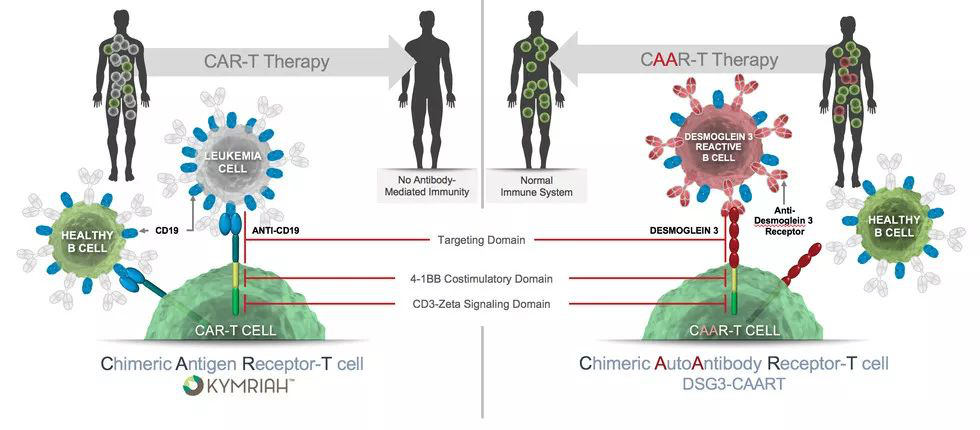
CAAR-T和CAR-T的异同
关于粘膜寻常型天疱疮(mPV)
寻常型天疱疮(一种孤儿病)是一种潜在致命的慢性自身免疫疾病,其特征在于皮肤和粘膜细胞之间粘附丧失。寻常型天疱疮是由靶向桥粒的特定致病性自身抗体引起的,桥粒是表皮中主要的细胞间粘附结构。PV有两种主要的临床形式:a.粘膜PV(mPV),仅由细胞粘附蛋白桥粒芯糖蛋白(DSG)3的自身抗体引起;粘膜皮肤PV(mcPV),由DSG3和DSG1的抗体引起。mPV占PV群体的约25%,其特征在于粘膜的疼痛性水疱,包括口,鼻,喉,食道,眼睛,生殖器和其他孔。粘膜皮肤PV影响其他75%的PV患者,并且还伴有皮肤水疱。
参考文献:
1. www.cabalettabio.com
2. Science. 2016 Jul 8; 353(6295): 179–184

