笔者在加入动脉网之后,因为接触的医药企业和医疗相关信息比较多,周围的朋友偶尔也会咨询一下医疗方面的问题。
得知徐寅(化名)的父亲病了,是在半年前。他当时找我咨询一下,有没有什么方法能够实现肿瘤早筛,想为家人定期做个体检。说起咨询的原因我才知道,徐寅的父亲被查出来肺癌晚期有一段时间了。为给父亲治病,他也一直在医院奔波。很多人都是因为身边的亲友得了肿瘤,才会去关注早筛的问题。
在他父亲的病情确诊之后,徐寅就如实告诉了父亲。徐寅想让父亲极配合医生治疗,一起面对这种凶险的疾病。“没有患者的配合,再好的治疗手段,也无法发挥最佳的效果。”徐寅这样认为。
老徐75岁,确诊时肺部的肿瘤已经有10几公分了。而且他身体不太好,医生没有考虑通过手术对肿瘤进行切除。后续的治疗方案,是在用化疗的方式在控制肿瘤。经过几次治疗后,老徐的身体逐渐消瘦。虽然化疗的副作用很大,但是老徐一直配合着医生完成了几期的治疗。
好景不长,2018年11月的一次CT检查,医生说老徐的肿瘤已经转移到了脑部。医生建议老徐做一个中子刀,先清除脑部的肿瘤。
在这之后,老徐的状态也越来越差,已经没有了行动能力。2019年1月,徐寅带着卧床不起的父亲,又一次住进了医院。虽然心里早已做好了准备,但是真正要面对这个时刻的来临时,他还是不太能够接受。这时,医生告诉徐寅,有一种针对肿瘤的特效药在去年12月底获批,就是信达药业即将上市的信迪利单抗,不知道他是否愿意试一试。
在老徐住院期间,医生向徐寅介绍了PD-1治疗方案,用信迪利单抗联合紫杉醇治疗。医生告诉徐寅,目前PD-1已经有国产和进口的几种药上市,综合对比价格之后,推荐使用信达生物的信迪利单抗——一款名字叫做达伯舒的国产生物创新药。
医生介绍到,配合药企买3赠2的方案,可以大幅度减小患者所承担的费用。徐寅这是第一次听说PD-1,他在手机上查询了解了PD-1药物对各种肿瘤的神奇效果之后,立即同意了这个治疗方案。虽然一个月的治疗花费在2万元左右,但是他还想为父亲做一些争取。
这款药虽然已经获批,但要到2月才正式上市,当时还无法从医院的药房拿到药。因为老徐的情况不佳,必须抓紧治疗,医生提出先提前使用赠药的方案,联系厂家使用免费的针剂进行注射。
在完成两次PD-1治疗之后,老徐的状态有了很明显的改善。从卧床不起,到可以下床走动,只用了1个多月的时间。甚至在2019年春节后,老徐和小梁一起,到小区外吃了一顿久违的火锅。
说实话,徐寅在1月几乎已经做好了最坏的打算。但是神奇的是,肺癌晚期脑转移的父亲,竟然一步步有所好转。
3月,徐寅带着已经完成三次治疗的父亲到医院做检查。CT显示,老徐的肿瘤面积从3126mm2,缩减到1448mm2,横截面积缩小了一半。
随后的肺癌肿瘤标志物检查,从2月到4月,癌胚抗原已经趋于正常。副作用是出现了皮肤瘙痒的症状,正通过激素进行治疗。这时候,徐寅想到了和朋友一起分享这个喜悦,也告诉了我他父亲的近况。
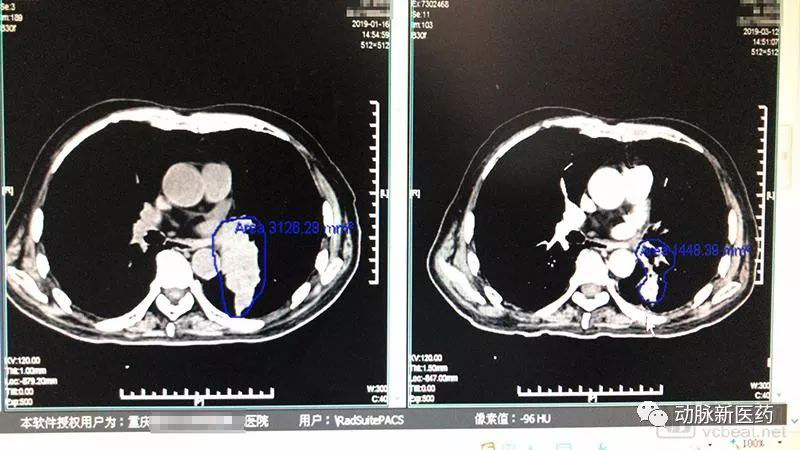
左图为1月15日CT结果,右图为3月12日CT结果,蓝圈内的肿瘤面积明显缩小。
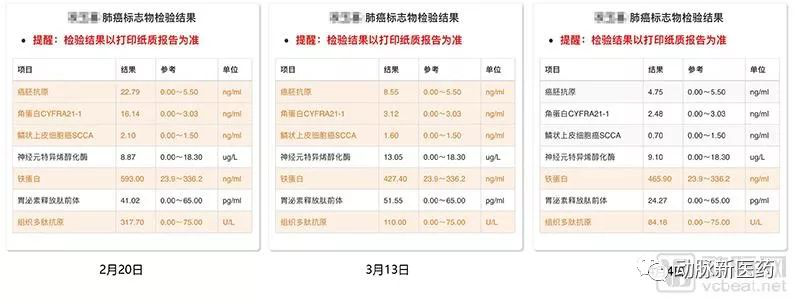
肺癌标志物检查各项指标在逐渐降低
听到朋友父亲的状态越来越好,我的心里也由衷为他高兴。但是,我详细地询问了医生给徐寅所交代的信息后,发现了问题。医生在超适应症使用PD-1,而且没有告知患者。
于是,我把我所了解的国内PD-1单抗的消息,都详细告诉给了徐寅。
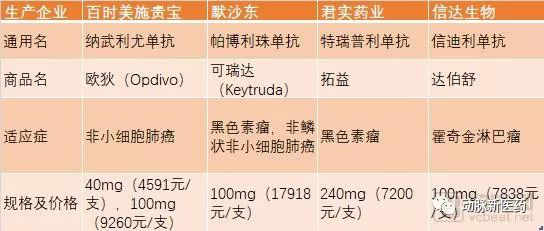
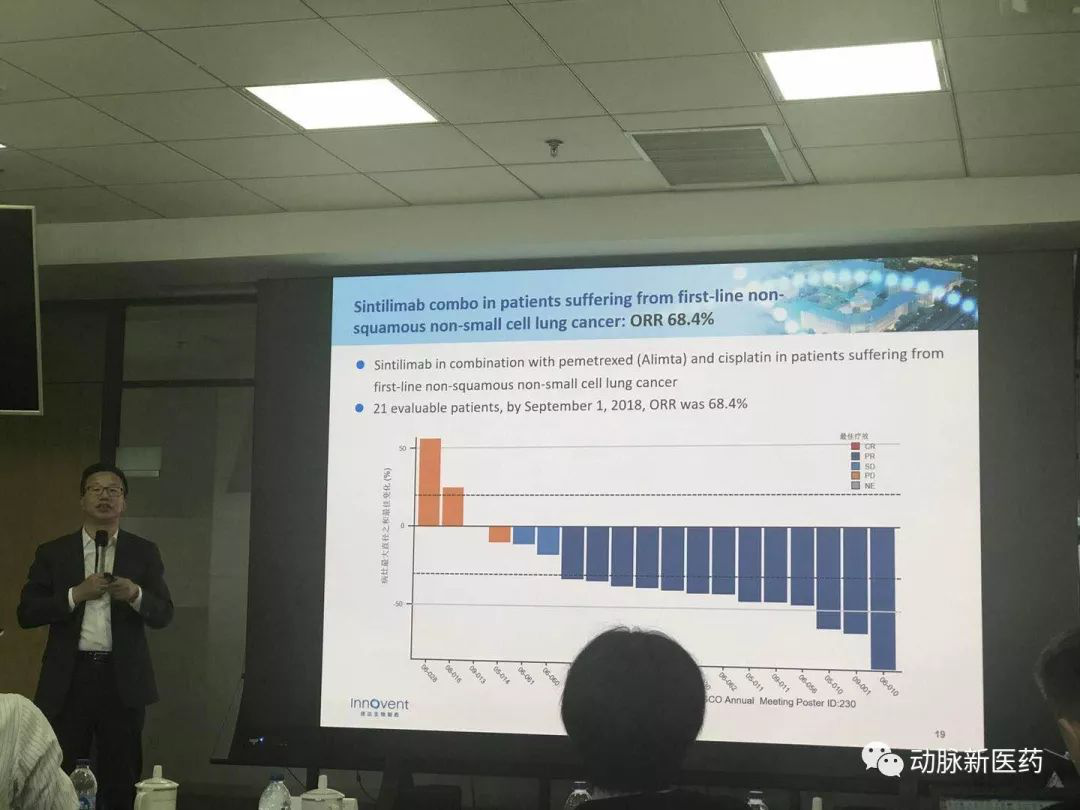
国内已经上市的四款PD-1单抗情况 当前国内已经上市的PD-1单抗一共有四种,两种进口药和两种国产药。进口药分别是默沙东的Keytruda(可瑞达)、百时美施贵宝的Opdivo(欧狄沃),国产药分别是君实生物的拓益和信达生物的达伯舒。 虽然K药和O药在国外已经拿下了不少肿瘤的适应症,但是在国内上市时都只获批了一种。百时美施贵宝的O药是第一个登陆国内市场的PD-1单抗,它首次获批的适应症是晚期非小细胞肺癌,K药首次获批的是恶性黑色素瘤,在2019年3月才新增了非鳞状非小细胞肺癌。 而国产PD-1拓益的适应症是用于既往接受标准治疗失败的局部进展或转移性黑色素瘤的治疗,达伯舒的适应症是复发或难治性经典型霍奇金淋巴瘤。当时适合老徐的,在国内被批准用于治疗晚期非小细胞肺癌的只有O药。 首先,不同的PD-1药物治疗范围是有差别的,不是什么肿瘤都能治疗。 其次,PD-1即使拥有对应的适应症,临床试验中也不是100%有效。而且,肿瘤的治疗有效并不等于完全治愈,如果医生没有准确告知,后续可能会为医生、医院带来严重的后果。 以进口的PD-1单抗默沙东K药为例,自2014年首次被美国FDA获批用于恶性黑色素瘤治疗以来,已在美国陆续获批15个肿瘤治疗适应症,覆盖十多个瘤种。 K药虽然已经经过循证医学的手段证实能够治疗很多其他瘤种,但是目前在中国目前仅获批了两个适应症,包括恶性黑色素瘤和非鳞状非小细胞肺癌,肺癌也是在3月28日才获批。因为K药在国内外良好的口碑,在国内超适应症使用的情况很多,这就是目前PD-1在临床使用中面临的主要问题。 君实生物和信达生物的PD-1,目前获批的适应症在中国都是小瘤种。肺癌才是中国癌症患者占比最高的癌症类型,每年发病人数接近80万例,其中80%~85%为非小细胞肺癌(NSCLC)。只有拿下肺癌的适应症,才能打开最大的肿瘤治疗市场。 虽然从适应症来看,达伯舒的治疗范围并不包含肺癌。但是我们知道,达伯舒正在进行多癌种的临床试验,肺癌临床试验也来到了Ⅲ期,治疗效果很好,企业也会为药品扩大适应症范围。 而且从老徐的状况看,达伯舒的确已经发挥了作用,只是医生并没有把情况为徐寅完全解释清楚。如果发生了治疗无效的情况,难免会产生医患矛盾。 PD-1超适应症用药,在国内已经非常普遍 百度PD-1贴吧里,还有大量的人在咨询是否可以选择国产PD-1超适应症使用。主要原因就是PD-1在肿瘤广谱治疗上的优秀表现,这些患者或者患者的亲属都想以身试药,增加生存的几率。另外,国产PD-1价格仅有进口药的三成,患者的经济压力大大减少,医生和患者家属都想用更小的代价去尝试拯救生命。 广东省肺癌研究所名誉所长、广东省人民医院终身主任吴一龙教授和中国抗癌协会肺癌专业委员会主任委员、上海交通大学附属胸科医院肿瘤科主任医师陆舜教授在之前关于此话题的一次采访中对国内超适应症应用PD-1/PD-L1单抗表达了担忧(参考文章链接:PD-1单抗扎堆获批,警惕滥用!)。 陆舜教授谈到:“目前还没有证据证明PD-1/PD-L1单抗都一样,也没有证据证明它们在临床上可以互换。”每个药都有各自获批的适应症,而这些适应症获批的依据是非常强烈和令人信服的临床试验的结果;只有循证医学数据的证据非常强,国家药品监管部门才会批准适应症。如果一个药还没有获批适应症的话,那说明这个药物还没有给出足够的循证医学数据。 吴一龙教授谈到,为了解决临床实际问题和药物可及性,临床上的确有超适应症用药的情况。如果一个药在国际上已经有临床试验结果,国际上也已经有药品监管部门批准了适应症,而中国因为各种情况,导致药物已经上市但某些适应症还没有获批,在这种特殊情况下使用问题不大。 但是,如果一个药在国外没有获批适应症,在国内也没有获批适应症,这是不可以在临床上使用的。从这个角度上来,严格按适应症用药,是为了保护医生和患者。 达伯舒虽然还没有拿到肺癌的适应症,但是也不能说这款药对肺癌患者无效。在动脉网参加的一次内部分享中,信达生物董事长俞德超展示过一组数据,信迪利单抗联合培美曲塞/顺铂一线治疗非鳞NSCLC的Ib期研究中显示,ORR可达到68.4%。 信迪利单抗联合吉西他滨/铂类双药一线治疗鳞状NSCLC的Ib期研究结果显示,ORR达到64.7%。信迪利单抗第2个提交上市的适应症就会是非小细胞肺癌适应症,时间大约在2020年前后。 2018年9月14日卫健委发布的《新型抗肿瘤药物临床应用指导原则》中,首次明确了临床超适应症应用新型抗肿瘤药物的界限,并界定了使用这些药物的医生必须具备的资质。也就是说,在我朋友徐寅父亲的案例上,医生是违规的。 而在后续和徐寅交流时,他也表示,即使当时医生说清楚,他也会选择使用PD-1,毕竟在当时的情况下,已经没有其他可以挽救父亲生命的选择了。而对症的O药昂贵的价格,他还暂时无法承受。而他更希望的是,要是这款国产药能早上市几个月就好了。那时他父亲的病情发展没有这么快,治疗后的效果可能会更好。 从目前的临床试验的数据来看,我们相信国产PD-1适应症范围也会逐步升级覆盖更多的瘤种。但是在这个特殊的时间点里,超适应症用药仍然是PD-1临床使用中无法掩盖的问题。我们只有期待这些PD-1单抗的适应症审批能够加速,普惠更多患者。