近日,MorphoSys公司宣布,该公司开发的tafasitamab与lenalidomide联用,在治疗复发/难治性弥漫性大B细胞淋巴瘤(DLBCL)患者的2期临床试验中达到试验主要终点。Tafasitamab是一款Fc端经过优化的抗CD19单克隆抗体。

DLBCL是最常见的非霍奇金淋巴瘤(NHL)类型,占B细胞NHL的40%。它是一种进展迅速的NHL类型。30-40%的患者对初始疗法没有反应或出现复发。对于复发/难治性DLBCL患者来说,他们通常需要接受强力化疗或者自体干细胞移植疗法。然而很多患者不能接受这些疗法,他们需要更多治疗选择。
Tafasitamab是一种靶向CD19抗原的人源化单克隆抗体。CD19是在B细胞癌症中广泛表达的抗原,它能够增强B细胞受体介导的信号通路,支持B细胞生存。它是靶向B细胞癌症的重要靶点。
MorphoSys公司对tafasitamab的Fc端进行了优化,增强了它引发抗体依赖性细胞介导的细胞毒性(ADCC)和抗体依赖性细胞吞噬(ADCP)的能力。在临床前模型中,tafasitamab能够通过与CD19结合,直接导致细胞凋亡。美国FDA曾授予这一疗法突破性疗法认定,用于治疗复发/难治性DLBCL患者。
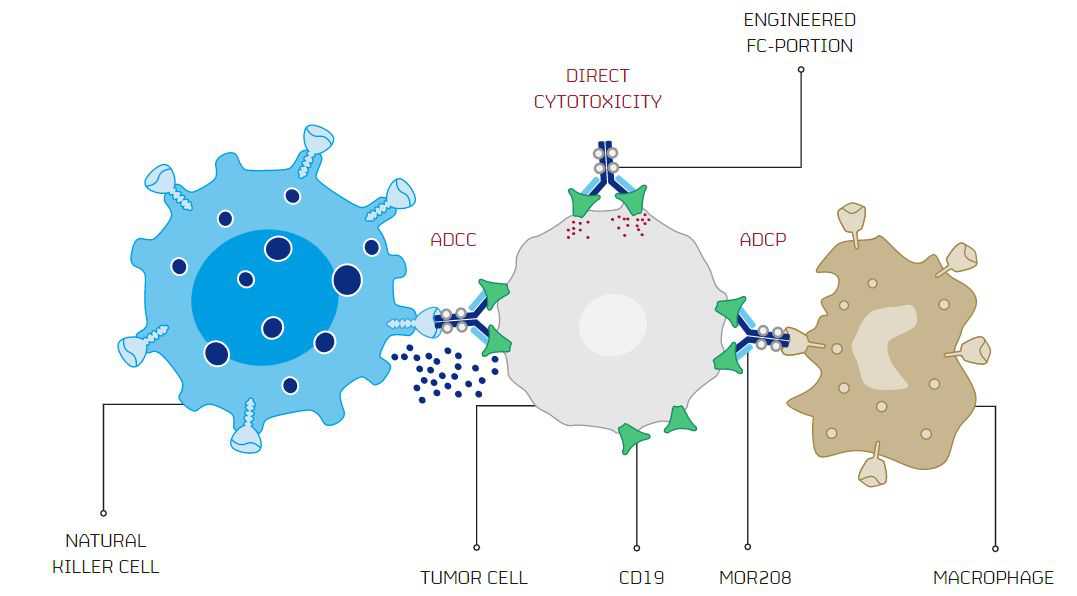
▲Tafasitamab作用机制(图片来源:MorphoSys公司官网)
在这项名为L-MIND的2期临床试验中,80名复发/难治性DLBCL患者接受了tafasitamab与lenalidomide构成的组合疗法的治疗。这些患者不适用于接受强力化疗或者干细胞移植疗法。试验结果表明,接受治疗的患者达到60%的客观缓解率(ORR),43%的完全缓解率(CR)。在中位随访期为17.3个月时,患者的中位无进展生存期(PFS)为12.1个月。
“我们对L-MIND试验的结果非常满意,它验证了我们在美国血液学会2018年会上公布的数据,”MorphoSys公司首席开发官Malte Peters博士说:“我们坚信我们拥有一款出众的候选药物。我们将致力于在今年年底之前向美国FDA递交生物制剂许可申请(BLA)。”
参考资料:
[1] MorphoSys AG: Primary Endpoint of L-MIND, a Combination Study of Tafasitamab (MOR208) and Lenalidomide, has been met, Confirming Previously Published Activity. Retrieved May 17, 2019, from https://www.morphosys.com/media-investors/media-center/morphosys-ag-primary-endpoint-of-l-mind-a-combination-study-of

