根据国家药监局药品审评中心(CDE)网站最新公示,有3款癌症治疗领域的新药拟纳入优先审评,分别是恒瑞医药的注射用卡瑞利珠单抗、豪森药业的甲磺酸奥美替尼片和武田的注射用维布妥昔单抗。值得一提的是,恒瑞医药昨日刚刚宣布PD-1单抗注射用卡瑞利珠单抗获批,又拟被纳入优先申请,业内推测其新适应症有望加速获批。

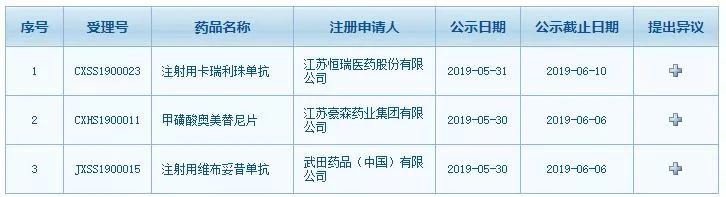
▲图片来源:国家药监局药品审评中心网站截图
恒瑞医药的注射用卡瑞利珠单抗
卡瑞利珠单抗是恒瑞医药自主研发的人源化抗PD-1抗体。昨日,恒瑞医药宣布卡瑞利珠单抗正式在中国获批,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(cHL)患者的治疗。

根据公开资料,目前恒瑞医药正在中国开展评估卡瑞利珠单抗单药或联合不同的治疗手段的29项研究。其中,2019年4月,注射用卡瑞利珠单抗联合阿帕替尼一线治疗晚期肝细胞癌3期临床研究在中国大陆地区、韩国、美国、欧洲和中国香港、中国台湾地区同步开展。(推荐相关阅读:抗击癌症!中国PD-1免疫联合疗法开发取得这些新进展)
豪森药业的甲磺酸奥美替尼片
豪森药业的1类新药甲磺酸奥美替尼片(HS-10296)是第三代EGFR抑制剂,根据该公司早前在港交所的招股书披露信息,该药拟用于治疗局部晚期或转移性非小细胞肺癌(NSCLC)患者(针对EGFR T790M耐药突变)。
武田的注射用维布妥昔单抗
维布妥昔单抗(brentuximab vedotin)是一种全新的抗体偶联药物(ADC),靶向治疗CD30阳性的淋巴瘤。该药分别于2015年和2017年先后在美国获批用于治疗霍奇金淋巴瘤(HL)和系统性间变性大细胞淋巴瘤(sALCL),以及皮肤间变性大细胞淋巴瘤(pcALCL)和表达CD30的蕈样肉芽肿(MF)的成人患者。
在若干研究报告中显示,相对于现有化疗治疗方案,维布妥昔单抗能够显著提高患者的生存,包括复发/难治性霍奇金淋巴瘤与系统性间变大细胞淋巴瘤,分别将5年生存率提高至41%与60%。

