近日,国家药监局药品审评中心(CDE)网站临床试验默示许可栏目公布了最新进展,又2款抗癌治疗领域的药品获得临床试验默示许可,分别为:
石药集团中奇制药技术(石家庄)有限公司的SYHA1807胶囊,用于晚期小细胞肺癌。该项目是一款1类化药,目前暂无更多公开信息。
徐诺药业(Xynomic Pharmaceutical)的对甲苯磺酸艾贝司他片(abexinostat),治疗恶性血液病。两个具体适应症为:既往接受过至少2种系统性治疗的复发或难治性滤泡性淋巴瘤(FL),以及既往接受过至少2次系统性治疗的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)。

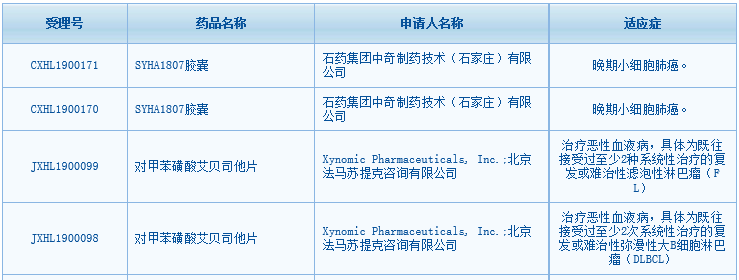
▲图片来源:国家药监局CDE官网
截至目前,对甲苯磺酸艾贝司他片已有3个适应症在中国获批临床。在此之前,对甲苯磺酸艾贝司他片用于治疗局部晚期或转移性肾细胞癌(RCC)的适应症已经在中国获批临床。
根据徐诺药业官网资料,对甲苯磺酸艾贝司他片是一款治疗血液肿瘤和实体瘤的创新的组蛋白去乙酰化酶(HDAC)抑制剂,具有同类最佳的潜力。该药已经在美国、欧盟和亚洲完成了17个临床1期和2期试验,显示了其对多种肿瘤具有临床疗效,并且在同类组蛋白去乙酰化酶抑制剂产品中具有更好的整体安全性。
公开资料显示,该药在全球领域的数个适应症正在开展临床研究。值得一提的是,其与帕唑帕尼(pazopanib)联合治疗局部晚期或转移性肾细胞癌(RCC)患者,已获得美国FDA快速通道资格;其用于治疗r/r滤泡淋巴瘤的单药疗法,已获得美国FDA加速批准资格。

▲图片来源:徐诺药业官网
徐诺药业总部在上海,专注于在全球授权引进、开发抗肿瘤新药。2018年5月,公司宣布在上海成立研发创新中心,以发现并开发聚焦激酶抑制、免疫肿瘤和表观遗传修饰等领域的小分子肿瘤药物,并于同年6月宣布完成B轮融资,用于在未来12个月内启动八项临床试验。

