今日,中国国家药监局药品审评中心(CDE)最新公告,8款新药的上市申请,共计13个受理号拟纳入优先审评程序。其中,博雅生物的人凝血酶原复合物、南岳生物的人凝血因子Ⅷ,以及诺和诺德(中国)的注射用重组人凝血因子Ⅷ,均为血友病治疗药物。在去年中国发布《第一批罕见病目录》中,血友病被纳入其中。因此,此次三款新药拟纳入优先审评的理由,均为按优先审评范围(二)4款罕见病纳入优先审评程序。
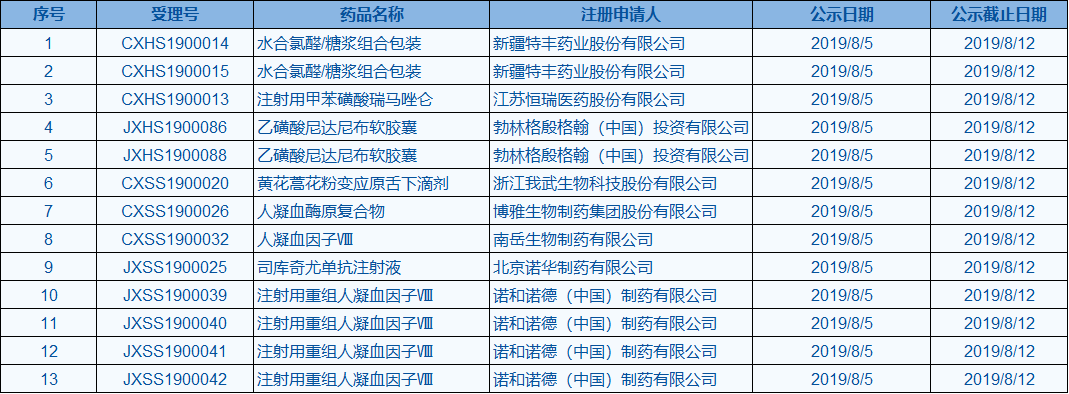
▲资料来源:CDE官网
血友病是一种X连锁的单基因隐性遗传病。它的特征是血液凝结级联反应受到破坏。A型血友病中的FVIII缺失,B型血友病中的凝血因子IX(FIX)缺失,导致失控的出血事件。重复的关节出血会导致关节疼痛,活动幅度受限,乃至永久性的关节损伤,进而严重影响血友病患者的生活质量。当前,血友病的主要疗法是通过定期输液来补充血液中缺乏的凝血因子。虽然这种疗法能够将患者的预期寿命提高到只比正常人少10年,但定期输液的负担和为了预防出血而谨小慎微的生活将陪伴他们一生。通过化学修饰延长凝血因子的半衰期,可以帮助血友病患者减少输液次数,减轻他们的治疗负担。
根据世界卫生组织(WHO)和世界血友病联盟(WHF)统计,目前中国约有10万人患有血友病,且每五年按70%增长。可见,血友病治疗药物在中国的临床需求是巨大的。目前,中国已上市治疗A型血友病的药物有人凝血因子Ⅷ,注射用重组人凝血因子Ⅷ,注射用重组人凝血因子Ⅶa;治疗血友病B的药物主要有注射用重组人凝血因子Ⅸ,注射用重组人凝血因子Ⅶa,人凝血酶原复合物。
人凝血酶原复合物系由健康人血浆经分离、提纯,并经病毒去除和灭活处理等工艺制成的血浆蛋白制品。根据博雅生物公告,该产品含有维生素K依赖的在肝脏合成的四种凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ。维生素K缺乏和严重肝脏疾患均可造成这四个因子的缺乏,而上述任何一个因子的缺乏都可导致凝血障碍。人凝血酶原复合物主要用于治疗先天性和获得性凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ缺乏症,如B型血友病等。2016年底,该药获得药物临床试验批件。
由南岳生物研发的凝血因子Ⅷ主要用于防治A型血友病和获得性凝血因子Ⅷ缺乏而致的出血症状及这类病人的手术出血治疗,该产品曾被列入中国国家“十二五”新药创制重大专项。南岳生物制药有限公司始建于1968年,具有三十四年血液制品安全生产历史,是中国首批血液制品生产企业之一。目前,该公司主要产品有:人血白蛋白、静注人免疫球蛋白(PH4)、人免疫球蛋白、乙型肝炎人免疫球蛋白、破伤风人免疫球蛋白、狂犬病人免疫球蛋白。

由诺和诺德开发的第三代重组凝血因子Ⅷ产品(turoctocog alfa,商品名:Novoeight)是一款用于治疗A型血友病的药物。Turoctocog alfa是一个B域载断重组人凝血因子Ⅷ,利用了最新的基因重组及蛋白纯化技术,于2013年10月获美国FDA批准上市。同时,诺和诺德还在该药的基础上,将分子量约为40kDa的PEG修饰在其B结构域上,将药物的半衰期提高了接近2倍,从而开发出另一款新药Esperoct。今年2月,Esperoct在美国获批上市,用于成人和儿童A型血友病患者的预防性治疗和急性治疗。
由诺华公司开发的司库奇尤单抗,是目前全球首个且唯一一个全人源IL-17A抑制剂。该药首次将治疗靶点集中于IL-17A这一银屑病核心致病因子上,能特异性结合任何来源的IL-17A而不妨碍其他细胞因子正常工作。银屑病是一种免疫相关的慢性、复发性、炎症性、系统性疾病。目前,银屑病在中国的发病率约为0.47%,患者人数超过650万,治疗需求远未被满足。今年4月,司库奇尤单抗在中国获批上市,用于治疗符合系统治疗或光疗指征的中度至重度斑块状银屑病的成年患者。这是2018年CDE发布《第一批临床急需境外新药名单》中首个获批的银屑病生物制剂。全球100项真实世界和临床研究证明,每10位患者中就有8位可通过16周司库奇尤单抗治疗实现皮损清除或几乎清除,患者应答率可近100%维持长达5年。
水合氯醛为催眠药、抗惊厥药。临床上,该药用于治疗失眠,麻醉前、手术前和睡眠脑电图检查前用药,以及用于癫癎持续状态的治疗,也可用于小儿高热、破伤风及子癎引起的惊厥。此次特丰药业的水合氯醛/糖浆组合包装的上市申请,拟按优先审评范围(二)6款儿童用药纳入优先审评程序。可以看出由特丰药业开发的水合氯醛/糖浆组合包装为一款适用于儿童的抗惊厥药品。
甲苯磺酸瑞马唑仑是恒瑞医药的1.1类新药,是一种短效GABAa受体激动剂,属于苯二氮卓类中枢神经系统药物。该产品用于患者的静脉麻醉,适应症可扩展至镜检时镇痛、术前麻醉和ICU镇静。此次,甲苯磺酸瑞马唑仑的上市申请拟按优先审评范围(一)3款具有明显治疗优势创新药纳入优先审评程序。若能获得优先审评,将缩短该药等待审批的时间和整体注册周期,为产品尽快上市创造有利条件。
尼达尼布(nintedanib)是勃林格殷格翰公司开发的一种口服三联血管激酶抑制剂,2014年10月经FDA批准该药用于治疗特发性肺纤维化(IPF),成为首个获准用于治疗IPF的酪氨酸激酶抑制剂(TKI)。尼达尼布针对已被证实在肺纤维化病理机制中具有潜在影响的生长因子受体发挥作用,其中最为重要的就是血小板源性生长因子受体(PDGFR)、成纤维细胞生长因子受体(FGFR)和血管内皮生长因子受体(VEGFR)。通过阻断这些参与纤维化进程的信号转导通路,尼达尼布能够通过减少肺功能下降速度、从而减缓IPF疾病进展。2017年9月,尼达尼布在中国获批上市,用于治疗特异性肺纤维化。这也是勃林格殷格翰2017年继阿法替尼、恩格列净之后在中国上市的第3款新药。此次,该药的上市申请拟按优先审评范围(一)3款具有明显治疗优势及(二)4款罕见病药品注册申请纳入优先审评程序。
黄花蒿花粉变应原舌下滴剂主要用于蒿属花粉过敏引起的变应性鼻炎(合并或不合并结膜炎、哮喘)的脱敏治疗。2012年,该药物获得NMPA颁发的《药物临床试验批件》。变应性鼻炎又称变态反应性鼻炎,是特应性患者接触过敏原后,由IgE(是指人体的一种抗体,存在于血中。是正常人血清中含量最少的免疫球蛋白,可以引起I型超敏反应)介导的组胺等介质释放、并有多种免疫活性细胞和细胞因子等参与的鼻黏膜慢性炎症反应性疾病,以鼻痒、喷嚏、鼻分泌亢进、鼻黏膜肿胀等为主要特点。此次,我武生物开发的黄花蒿花粉变应原舌下滴剂的上市申请,拟按优先审评范围(一)3款具有明显治疗优势创新药纳入优先审评程序。



