七夕情人节,牛郎会织女。在肿瘤学领域,不少以PD-1为代表的免疫检查点抑制剂似乎也到了“青春期”,正在寻找适合自己的“对象”,以期扩展这一创新疗法的疗效和适用范围。今年3月,默沙东的PD-1抑制剂帕博利珠单抗(Keytruda)联合化疗在中国获批一线治疗非小细胞肺癌(NSCLC)。在代号为Keynote-189的临床试验中,联合用药总缓解率是单用化疗的两倍以上,同时死亡风险降低了51%!对于晚期肺癌患者而言,这是极大的进步。作为中国首个PD-1抗体“牵手”成功的案例,帕博利珠单抗+化疗的组合给中国开发PD-1的企业不少信心。今天,我们就来“八卦”一下,中国已经获批上市的PD-1抗体们,都有哪些“牵手对象”。
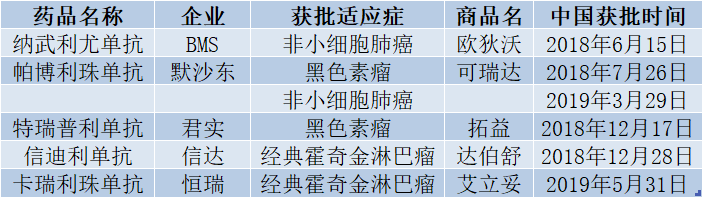
▲中国已获批上市的PD-1抗体(表格由医药观澜整理,数据来源:China drug trials)
拓展阅读:抗击癌症!中国PD-1免疫联合疗法开发取得这些新进展

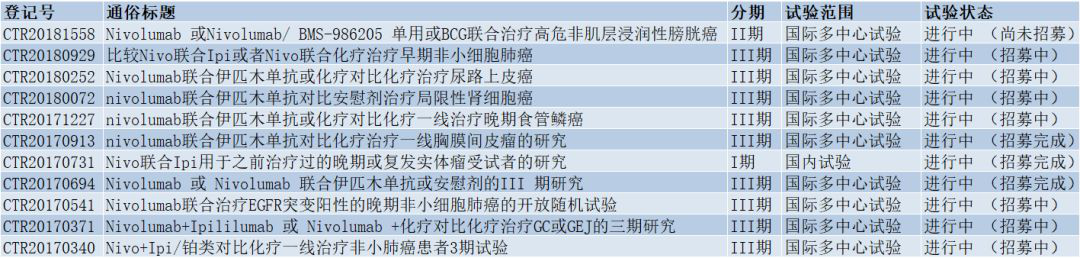
▲正在中国开展的联合疗法临床试验一览(表格由医药观澜整理,数据来源:China drug trials)
由百时美施贵宝(BMS)开发的纳武利尤单抗是中国第一款获批上市的PD-1抑制剂,其在中国开展最多的联合疗法组合是与伊匹木单抗联用。后者是一款抗CTLA-4单克隆抗体,也是一款免疫检查点抑制剂。在药物临床试验登记与信息公示平台上,该组合共登记了10项临床试验,适应症包括NSCLC、尿路上皮癌、肾细胞癌、食管鳞癌、胸膜间皮瘤、小细胞肺癌和胃癌或胃食管交界处癌,且大多数为国际多中心3期试验。事实上,纳武利尤单抗+伊匹木单抗的组合也是全球首个获得监管机构批准的免疫肿瘤药物联合疗法,已在美国获批治疗黑色素瘤、结直肠癌、以及肾癌。在一项名为CheckMate 067的3期临床研究中,该组合取得了亮眼的结果:相比CTLA-4、PD-1单药治疗,联合这两种药物治疗晚期黑色素瘤患者的死亡风险分别下降了46%和35%。
BMS在中国开展了一项纳武利尤单抗联合IDO1抑制剂BMS-986205治疗高危非肌层浸润性膀胱癌的2期试验。BMS-986205是一款全新的IDO1抑制剂。在一项名为CA017-003的1/2a期临床试验中,BMS-986205与Opdivo的组合有效彰显出了抗癌潜力。在25名接受过大量治疗的膀胱癌患者中,这一组合取得的客观缓解率和疾病控制率分别为32%和44%。

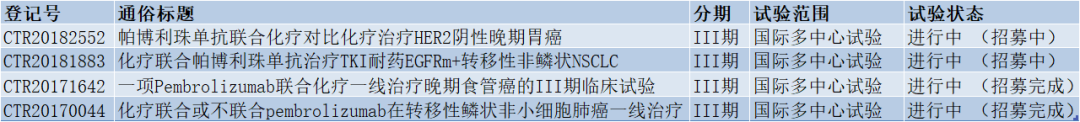
▲正在中国开展的联合疗法临床试验一览(表格由医药观澜整理,数据来源:China drug trials)
牵手对象1:化疗
在中国,由默沙东(MSD)开发的帕博利珠单抗联合最多的便是化疗。在药物临床试验登记与信息公示平台上,该药共登记了4项该联合疗法的临床试验,这些临床试验均为国际多中心3期研究。适应症除了已获批的非小细胞肺癌(NSCLC)外,还有晚期胃癌和食管癌。
ClinicalTrials网站上显示,中山大学利用帕博利珠单抗加仑伐替尼的组合开展了5项针对晚期肝细胞癌的临床研究,其中1项已进入3期试验。另1项针对肝内胆管细胞癌的研究也已经开展。另外,北京协和医院也利用该组合在晚期肝胆肿瘤上进行了探索,包括恶性原发性肝癌和胆管癌。仑伐替尼是由日本卫材公司开发的多靶点VEGFR受体抑制剂,在美国已被批准用于一线治疗甲状腺癌、肾细胞癌和肝细胞癌等患者。该联合疗法用于晚期肾癌曾获得美国FDA授予的突破性疗法认定。
ClinicalTrials网站还登记了2项帕博利珠单抗联合细胞疗法的研究,均为比较单独的PD-1与PD-1加自体树突细胞-细胞因子诱导的杀伤细胞(DC-CIK)免疫治疗在晚期实体瘤患者中的临床疗效和毒性。

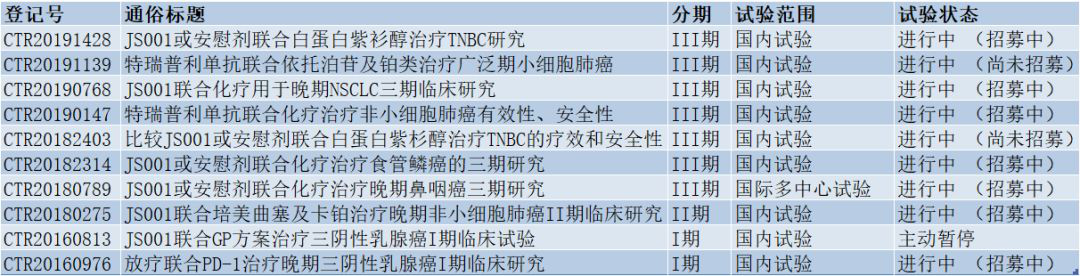
▲正在中国开展的联合疗法临床试验一览(表格由医药观澜整理,数据来源:China drug trials)
由君实生物开发的特瑞普利单抗,是中国获批上市的第三款PD-1抗体。与帕博利珠单抗类似,该药最常见的“牵手对象”也是化疗。在药物临床试验登记与信息公示平台上,该药共登记了9项该组合疗法的临床试验,其中7项已进展至临床3期。这些化疗方案包括培美曲塞及卡铂、白蛋白紫杉醇、依托泊苷及铂类、GP方案等;适应症涵盖NSCLC、小细胞肺癌、食管鳞癌、鼻咽癌、三阴乳腺癌。值得注意的是,君实生物在去年7月与石药集团达成了合作,双方将开展特瑞普利单抗与白蛋白紫杉醇组合用于治疗乳腺癌。
在药物临床试验登记与信息公示平台上,君实生物还开展了一项放疗联合特瑞普利单抗治疗晚期三阴性乳腺癌的前瞻性1期临床研究。目前,这项研究正在招募阶段,计划在中国招募54人。
君实生物曾与百泰生物达成合作,将其PD-1单抗特瑞普利单抗与后者开发的尼妥珠单抗联合用于晚期食管鳞状细胞癌,这是一项开放的2期临床研究。尼妥珠单抗是一种靶向EGFR的单克隆抗体,2018年在中国获批上市用于治疗头颈癌。
在2018年ASCO年会上,特瑞普利单抗联合阿昔替尼一线治疗晚期粘膜黑色素瘤的1b 期临床研究曾亮相。研究显示,对全部33例患者进行肿瘤评估,获得客观缓解率为 60.6%(20/33),疾病控制率达到87.9%(29/33)。阿昔替尼是一种口服的,作用于血管内皮生长因子受体1,2和3的强效和高选择性酪氨酸激酶抑制剂,2015年在中国被批准用于进展期肾细胞癌的成人患者。
去年11月,君实生物与和记黄埔医药签订合作协议,将探索特瑞普利单抗与索凡替尼联合治疗晚期实体瘤的效果。今年6月,索凡替尼胶囊与特瑞普利单抗注射液联合用药的1期临床试验申请获得临床试验默示许可。该组合疗法在ClinicalTrials网站上,一项编号为NCT03879057的1期临床研究正在进行中。索凡替尼是一款以血管细胞内皮生长因子受体 (VEGFR) 和成纤维细胞生长因子受体 (FGFR) 为靶点的选择性酪氨酸激酶抑制剂。
今年1月,贝达药业宣布其全资子公司卡南吉医药收到中国国家药监局(NMPA)签发的vorolanib(CM082)与特瑞普利单抗注射液联用的《临床试验通知书》,批准开展用于既往未经治疗的局部进展或转移性黏膜黑色素瘤的临床试验。CM082是贝达药业旗下的一款针对VEGFR和PDGFR靶点的多靶点受体酪氨酸激酶(RTKs)抑制剂,可抑制新生血管生成及肿瘤生长,并能克服同类靶向药常见的高毒副作用。
今年4月,亚盛医药与君实生物宣布达成一项战略合作协议。双方将针对亚盛医药特有的细胞凋亡抑制蛋白(IAP蛋白)抑制剂APG-1387与君实生物的抗PD-1单抗特瑞普利单抗的联合用药在中国大陆进行临床探索,治疗包括肿瘤(实体瘤与血液瘤),特别是难治性肿瘤、药物耐受性肿瘤等和其他双方另行确定的适应症。

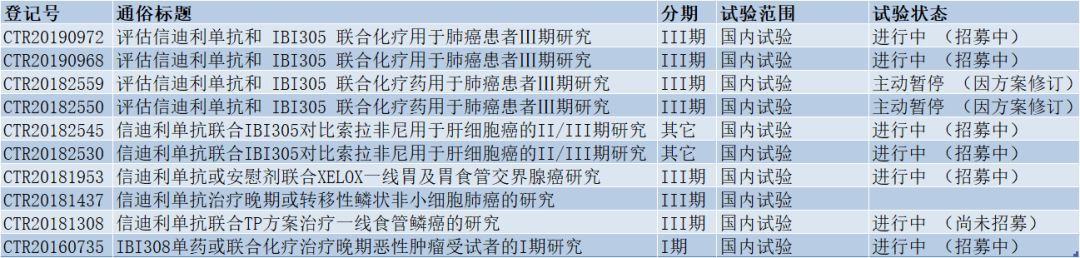
▲正在中国开展的联合疗法临床试验一览(表格由医药观澜整理,数据来源:China drug trials)
牵手对象1:IBI305
信达生物围绕信迪利单抗在中国开展最多的联合疗法组合是与其抗VEGF单抗IBI305联用。就在今天,该公司信迪利单抗联合IBI305临床研究招募一线晚期肝癌患者。IBI305是重组抗血管内皮生长因子(VEGF)人源化单克隆抗体注射液,据悉,该药已向NMPA申请上市。在药物临床试验登记与信息公示平台上,信达生物共登记了6项该组合的临床试验,适应症包括肺癌和肝细胞癌,其中4项已进展至临床3期。
牵手对象2:化疗
在药物临床试验登记与信息公示平台,信达生物还开展了4项信迪利单抗联合化疗的临床试验,适应症涉及NSCLC、胃及胃食管交界腺癌、食管鳞癌等。这些化疗方案有吉西他滨和铂类、XELOX方案、TP方案等。该联合疗法用于一线治疗晚期或转移性非小细胞肺癌(NCT02937116,队列D和队列E)的初步试验数据也在今年ASCO亮相。数据显示,队列D和队列E客观缓解率分别为68.4%和64.7%,中位无进展生存期分别为11.4个月和6.5个月。
牵手对象3:呋喹替尼
去年11月,和记黄埔医药与信达生物达成合作,将探索呋喹替尼与信迪利单抗联合用于多种实体瘤。呋喹替尼是一种新型的高选择性小分子VEGFR1、2及3抑制剂,已在中国获批用于治疗转移性结直肠癌。在临床试验默示许可公示中,呋喹替尼胶囊联合信迪利单抗的2/3期临床研究已被批准。
牵手对象4:西达本胺
信达生物曾与微芯生物达成临床合作研究。在ClinicalTrials网站上,登记了一项信迪利单抗与微芯生物自主研发的西达本胺联合用于复发/难治结外NK/T细胞淋巴瘤的1b/2期研究。西达本胺是一种组蛋白去乙酰化酶抑制剂(HDACi),2014年在中国获批上市。此外,该组合还将与IBI305联合用于晚期结直肠癌的治疗。

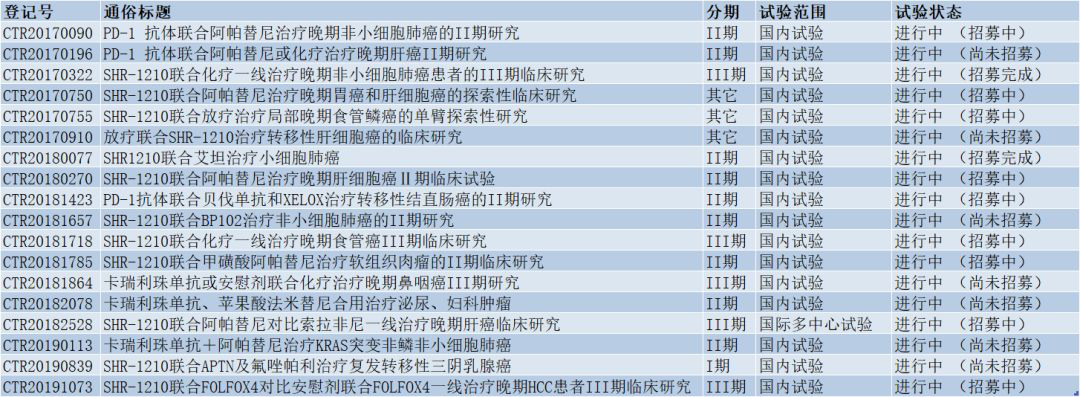
▲正在中国开展的联合疗法临床试验一览(表格由医药观澜整理,数据来源:China drug trials)
在中国,与卡瑞利珠单抗联合用药最多的是阿帕替尼。后者也是恒瑞医药创新研发的一款针对晚期胃癌的的小分子靶向药物,2014年在中国获批上市。在药物临床试验登记与信息公示平台上,恒瑞医药共登记了8项该组合的临床试验,其中6项为2期试验,涉及适应症包括NSCLC、小细胞肺癌、肝细胞癌、软组织肉瘤。在一项卡瑞利珠单抗联合甲磺酸阿帕替尼治疗晚期肝细胞癌、胃及胃食管结合部腺癌的1b期研究中,该组合治疗晚期肝细胞癌的客观缓解率高达 50%,6 周的疾病控制率达到 93%。
在药物临床试验登记与信息公示平台上,恒瑞医药开展了一项卡瑞利珠单抗与苹果酸法米替尼合用治疗泌尿、妇科肿瘤的2期临床试验。法米替尼是恒瑞医药开发的一款口服多靶点受体酪氨酸激酶抑制剂,具有抗增殖和抑制血管生成的双重抗肿瘤作用。目前,法米替尼针对结直肠癌患者的3期临床试验已完成,恒瑞医药已在中国递交新药上市申请。
卡瑞利珠单抗联合化疗也是一个常见组合。在药物临床试验登记与信息公示平台上,恒瑞医药开展了6项该组合的临床研究,化疗方案有XELOX方案和FOLFOX4方案,适应症包括NSCLC、肝细胞癌、结直肠癌、食管癌、鼻咽癌等。今年7月,恒瑞医药宣布卡瑞利珠单抗联合化疗的两项3期临床试验申请,收到NMPA核准签发的《临床试验通知书》,适应症分别为晚期或转移性胃癌(GC)或胃食管交界处癌(GEJ),及晚期肝细胞癌。
恒瑞医药在药物临床试验登记与信息公示平台上登记了2项卡瑞利珠单抗联合放疗的临床研究,适应症分别为食管鳞状细胞癌和肝细胞癌。
恒瑞医药在药物临床试验登记与信息公示平台上登记了2项卡瑞利珠单抗联合贝伐单抗的临床研究,适应症分别为NSCLC和结直肠癌。其中,贝伐单抗是一款抑制肿瘤血管生成的药,BP102是贝伐单抗的生物类似药。
恒瑞医药在药物临床试验登记与信息公示平台上登记了一项卡瑞利珠单抗联合甲磺酸阿帕替尼及氟唑帕利治疗复发转移性三阴乳腺癌的开放、多中心、剂量探索的1b期临床研究。目前,该研究正在进行中,尚未招募。
在一项编号为NCT03171220的研究中,恒瑞医药将其PD-1与新抗原反应性T细胞(NRTs)联合用于晚期难治性实体瘤患者。该研究已在2017年启动,计划在明年底完成。
在一项编号为NCT03527251的研究中,中山大学对卡瑞利珠单抗联合伊匹木单抗在NSCLC患者中展开了研究。这是一项始于去年5月的1期临床研究,计划招募10名受试者,预计将会在今年12月底完成研究。
除了上述盘点的5款已在中国上市PD-1抗体之外,其他正在临床开发阶段的其他同类产品也正在积极探索更有效的免疫组合。例如,百济神州在去年与Mirati公司达成合作,将开展对sitravatinib与百济神州的PD-1候选物替雷利珠单抗联合用药的研究,目前该研究已进展至1b期。今年4月,百济神州与BioAtla就有条件激活的CTLA-4抑制剂达成合作协议,其中一项合作内容便是测试CTLA-4与百济神州PD-1的联合疗法。据悉,百济神州已向NMPA递交了替雷利珠单抗用于经典型霍奇金淋巴瘤和尿路上皮癌2项适应症的新药上市申请。
同样是免疫检查点抑制剂,几款已在中国进展至临床后期的PD-L1抗体也在寻找组合疗法的路上。基石药业旗下肿瘤免疫药物PD-L1单抗CS1001一线联合化疗治疗胃腺癌或胃食管结合部腺癌的3期临床试验GEMSTONE-303已在今年4月实现首例患者给药。此外,该公司还分别与拜耳、英派药业等公司达成合作,以期开发CS1001联合口服多激酶抑制剂瑞戈非尼,以及CS1001联合PARP抑制剂IMP4297治疗多种癌症。
由罗氏开发的PD-L1单抗atezolizumab已向中国NMPA递交了上市申请。该药联合化疗治疗三阴乳腺癌的临床研究已进展至临床3期。此前3月,美国FDA已批准该联合疗法用于广泛期小细胞肺癌的一线治疗。该药还在中国开展了与贝伐珠单抗联合治疗肝细胞癌的3期研究。同样已向中国递交上市申请的PD-L1抗体还有阿斯利康旗下的durvalumab。该公司在今年6月宣布durvalumab的组合疗法在一线治疗广泛期小细胞肺癌的3期临床试验中,达到了试验的主要终点。目前,该药也在中国开展了与tremelimumab联合治疗肝细胞癌的2期研究。
与当下一夫一妻婚姻制不同的是,在肿瘤免疫领域并不要求PD-1/L1抗体要“专情”。只要两种疗法组合能够带来更好的(具有统计学意义)疗效,在安全性可以接受的前提下,这样的组合就能够得到认可。从上述盘点中也不难发现,一些靶向药物、化疗和放疗都是PD-1/L1的常见搭配。人们之所以热衷于推动免疫检查点抑制剂与其他疗法“牵手”,很大一个原因是这类药物作为单药疗法的响应率并不高(10%-35%)。正是如此,基于免疫检查点抑制剂的创新组合疗法正在成为这一领域的热点,同时也是很多公司的重要研发策略。随着科学的不断探索,相信更多“牵手”成功的免疫组合疗法能够获批上市,从而让更多患者获益其中。












