脊髓性肌萎缩症(SMA)是一种罕见的常染色体隐性遗传性神经肌肉疾病,其特点是进行性、使人衰弱的肌肉萎缩、无力。过去的几十年来,人类对这种疾病独特的分子遗传学和病理生理学的认识不断进步,为药物治疗提供了基础。2016年12月,首个SMA治疗药物诺西那生钠注射液(美国和欧盟注册商品名SPINRAZA®)在美国获批用于治疗儿童和成人SMA患者。2019年5月,ZOLGENSMA®在美国获批用于治疗2岁以下患有SMN1等位基因突变导致的SMA儿童患者。创新药物为SMA患者带来希望和治疗选择。从秉承科学严谨性和以患者为本的角度出发,本文对SMA治疗药物相关的两个关键问题予以阐述。
ZOLGENSMA® 的一次性给药用法是基于其美国批准的说明书,“ZOLGENSMA®只能使用一次,目前尚没有证据支持其二次注射的有效性和安全性”(ZOLGENSMA® Prescribing Information Initial US Approval 2019)。ZOLGENSMA®通过AAV9病毒载体引入人SMN1基因,在ZOLGENSMA®的临床试验中,仅入组了基线抗-AAV9抗体滴度≤ 1:50的患者,试验结束时抗-AAV9抗体至少升高至1:102,400,大部分患者滴度超过1:819,200,对于出现高抗-AAV9抗体滴度的患者再次给药尚未进行评估(ZOLGENSMA® Prescribing Information Initial US Approval 2019)。
“一次性给药”和“治愈”是完全不同的两个概念(英文为:single-dose 和 cure),“一次性给药”是基于药物本身特性的使用方法,“治愈”是治疗的结果,二者无必然联系,不能混为一谈。ZOLGENSMA®的临床试验CL-101中 15例患者(3例为低剂量组,12例为高剂量组)中的4例没有达到CHOPINTEND 评分大于40分(3例来自低剂量组,1例来自高剂量组);13例没有到最大评分64分,仅有2例达到64分;高剂量组中的9例可以独坐≥ 30秒;1例高剂量组的患者仅是获得了帮手送到嘴边的进步(Mendell J,2017)。同时,基于AAV的基因治疗的持久性尚未被很好的证实。基于AAV治疗其它疾病的基因治疗显示出有限的疗效持久性,有部分病人在一开始疗效达高峰后出现疗效下降(Bainbridge JWB,2015;BryantLM,2013;Cideciyan AV, 2013;Jacobson SG,2015;Wright AF,2015)。并且基因治疗安全性方面一直存在担心,因为一旦注射之后,即使出现严重的不良反应也不能停止其作用,目前尚无解毒剂(Kaemmerer WF, 2018)。综上所述,基于目前已有证据无法得出ZOLGENSMA®可以治愈SMA的结论。
2、 目前为止尚无ZOLGENSMA® 和SPINRAZA®之间头对头比较的研究
众所周知,如果要科学严谨地比较临床上两种治疗手段,需要设计严格的“头对头”的临床研究,但目前为止尚无ZOLGENSMA® 和SPINRAZA®之间头对头比较的研究,跨试验间的比较是不科学的。由于不同试验设计和研究人群的不同,研究结果是不具可比性的。比较并不匹配的SPINRAZA®的ENDEAR研究和ZOLGENSMA®的CL-101和STRIVE 研究是不科学的,会得出错误的结论并误导读者。
》》ENDEAR研究和CL-101及STRIVE研究的设计、证据级别是不同的。
ENDEAR是一项随机、双盲、假操作对照、多中心3期临床研究(Finkel RS,2017)。CL-101研究是一个开放、单臂1期临床研究(Mendell J,2017);STRIVE研究是一个开放、单臂3期临床研究(ZOLGENSMA® Prescribing InformationInitial US Approval 2019;ZOLGENSMA® Presented at AAN2019)。ENDEAR共入组了121例SMA1型患者,包括80例用SPINRAZA®治疗的患者,在ENDEAR 的最终分析时,121例患者纳入了事件发生时间分析,在所有其它分析中,纳入了末次访视前已经入组至少6个月的110例患者(Finkel RS,2017)。而CL-101研究共入组了15例SMA1型患者(Mendell J,2017),STRIVE研究共入组了21例SMA1型患者(ZOLGENSMA®Prescribing Information Initial US Approval 2019;ZOLGENSMA®Presented at AAN 2019)。ENDEAR研究的样本量远大于CL-101及STRIVE。
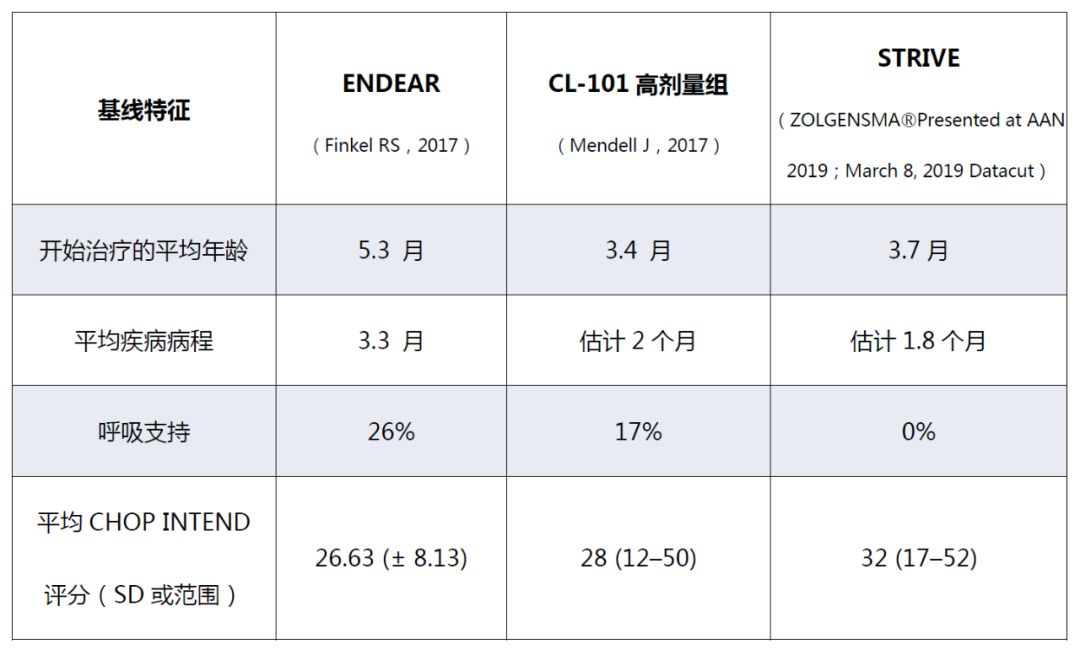
》》ENDEAR,CL-101及STRIVE的患者基线特征包括年龄、平均疾病病程、呼吸支持情况、以及CHOP INTEND评分都是不同的。SPINRAZA®的临床试验中共入组超过300例SMA患者(包括两个3期多中心、随机双盲对照研究)。截至2019年6月30日,全球已有超过8400名成人、儿童SMA患者接受了SPINRAZA®的治疗,最长长达6年。ZOLGENSMA®需要更多的数据来支持其长期的疗效以及安全性。