日前,辉瑞(Pfizer)公司在第28届欧洲皮肤病与性病学会(EADV)大会上公布,其JAK1抑制剂abrocitinib,在治疗12岁及以上中重度特应性皮炎(AD)患者的3期关键性临床试验JADE MONO-1中,达到了主要终点和所有关键性次要终点。辉瑞公司预计将在2020年向监管机构递交新药申请。特应性皮炎是一种慢性、复发性皮肤病,主要症状为身体任何部位可能出现严重瘙痒、皮肤干裂和炎症。中重度特应性皮炎患者因为严重瘙痒可能导致皮肤损伤和失眠。如同其它慢性炎症性疾病一样,特应性皮炎也是免疫系统介导的疾病,免疫细胞和炎症性细胞因子之间的复杂互动在疾病发生方面起到重要作用。作为最常见的慢性皮炎之一,它在世界范围内影响高达20%的儿童患者和10%的成年患者。而且在这些儿童患者里,有约一半会出现症状的反复。因此,他们需要一款新型药物来控制他们的病情。
辉瑞的abrocitinib是一种口服小分子特异性JAK1抑制剂。JAK1抑制剂通过调节多种与特应性皮炎病理相关的细胞因子来控制病情,包括白细胞介素IL-4,IL-13,IL-31和干扰素γ。之前,abrocitinib已经获得美国FDA授予的突破性疗法认定。
▲Abrocitinib的分子结构式(图片来源:ChemIDplus)该项名为JADE MONO-1的试验是一项随机,双盲,含安慰剂对照的3期临床研究,旨在评估abrocitinib对12岁及以上中重度特应性皮炎患者的有效性和安全性。参与该试验的387名患者被随机分配接受每日一次200毫克或100毫克的abrocitinib或安慰剂的治疗。试验结果表明,治疗12周后,与安慰剂组相比,分别有43.8%和23.7%的患者皮肤症状达到或接近完全消失(IGA评分0/1),而在安慰剂组的数值为7.9%。而且,在治疗组中,分别有62.7%和39.7%的患者的湿疹面积和严重程度指数比基线改变至少75%(EASI 75),而安慰剂组中这一数值只有11.8%,达到试验的主要疗效终点。
值得一提的是,美国FierceBiotech网站上发布的文章指出,该试验治疗组中57.2%的患者(200毫克剂量组)的瘙痒数字评定量表(NRS)评分至少提高四分,高于另一款生物制剂dupilumab在治疗16周后达到这一效果的患者比例,abrocitinib在患者的止痒方面可能具有潜在的优势。此外,abrocitinib还在该试验中达到了EASI 90等其它关键性次要终点。
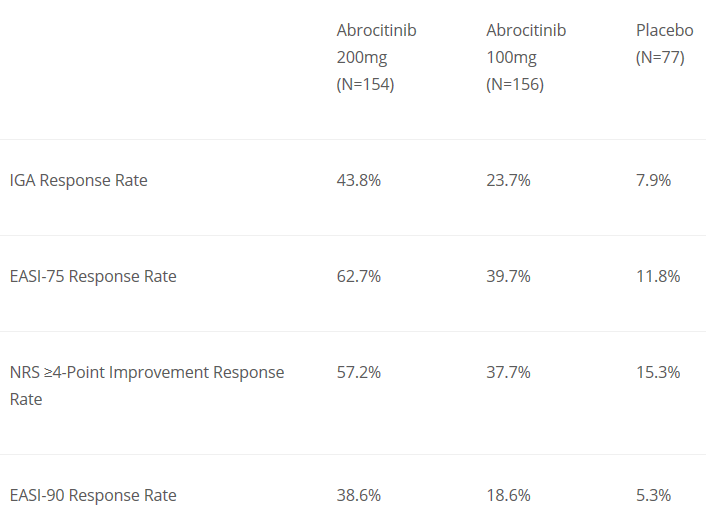
▲在JADE MONO-1试验中,abrocitinib达到主要终点和关键性次要终点的患者比例
“中重度特应性皮炎患者非常需要有效的治疗方案来改善他们的病情,”辉瑞全球产品开发部炎症与免疫学首席开发官Michael Corbo博士说:“治疗中重度特应性皮炎的两项关键性3期临床试验的积极结果证明了abrocitinib在改善患者病情方面的潜力。如果获得批准,abrocitinib可能成为这些患者的首款每日口服一次的治疗选择。”
参考资料:
[1] Pfizer Presents Positive Phase 3 Data at the 28th Congress of the European Academy of Dermatology and Venereology for Abrocitinib in Moderate to Severe Atopic Dermatitis, Retrieved October 14, 2019, from https://www.pfizer.com/news/press-release/press-release-detail/pfizer_presents_positive_phase_3_data_at_the_28th_congress_of_the_european_academy_of_dermatology_and_venereology_for_abrocitinib_in_moderate_to_severe_atopic_dermatitis
[2] Pfizer posts detailed phase 3 data on its Dupixent rival, Retrieved October 14, 2019, from https://www.fiercebiotech.com/biotech/pfizer-posts-detailed-phase-3-data-its-dupixent-rival



