医药投资:首款靶向Eta抗体药物!鸿运华宁肺动脉高压新药在中国获批临床
2019-10-28 10:59:08
10月24日,中国国家药监局药品审评中心(CDE)网站公示,鸿运华宁生物医药的重组抗人内皮素受体A人源化单克隆抗体注射液(GMA301)已获得临床默示许可,适应症为肺动脉高压。这是一款作用于内皮素受体ETa的抗体药物。根据鸿运华宁官网信息,目前全球仅有3款小分子ETa拮抗剂获批用于治疗肺动脉高压;而GMA301是首个作用于Eta的抗体候选药物开发用于该适应症。2017年该药还获得美国FDA授予的孤儿药资格。

▲截图来源:CDE官网
肺动脉高压被称为是“心血管系统中的癌症”,在中国俗称“蓝嘴唇”。这是一类罕见且危重的疾病,目前尚无法治愈。公开数据显示,全球范围约2500万患者,中国患者约100~200万人。研究表明,内皮素受体ETa抑制剂能有效的抑制肺动脉平滑肌细胞的增殖,阻断由内皮素引起的肺动脉压力增加,改善肺动脉高压病人的运动能力和血液动力学,缓解症状。目前全球有多款小分子ETa抑制剂获批,但在特异性和肝毒性方面尚存局限,临床上亟需特异性更强,毒性更低的治疗药物。作为全球首款靶向Eta开发治疗肺动脉高压的抗体药物,GMA301的作用机制在于,通过与内皮素受体Eta的结合,降低内皮素导致的血管压力增加,从而缓解肺动脉压力过高的症状。据悉,该药的靶向特异性良好,药效作用时间长,且无小分子药物所产生的肝毒性。它能够有效抑制或减缓右心和肺动脉的肥厚,进一步改善肺动脉高压患者运动耐量、生活质量和生存时间,有望成为治疗肺动脉高压的新一代长效药物,为患者带来新的治疗选择。据悉,此次该药在中国获得临床默示许可,是GMA301国际多中心临床试验的一部分。根据鸿运华宁今年5月的新闻稿,GMA301注射液的国际多中心临床试验预计将于2020年内结束。
鸿运华宁成立于2010年,致力于心脑血管和代谢系统的重大慢性疾病以及癌症的抗体新药研究、开发与产业化,该公司创始人、董事长兼首席执行官为景书谦博士。
目前,该公司已建立了丰富的在研产品管线。除了GMA301,其针对二型糖尿病的超长效GLP-1抗体激动剂GMA102以及针对肥胖症的在研产品GMA105均在开展临床研究。
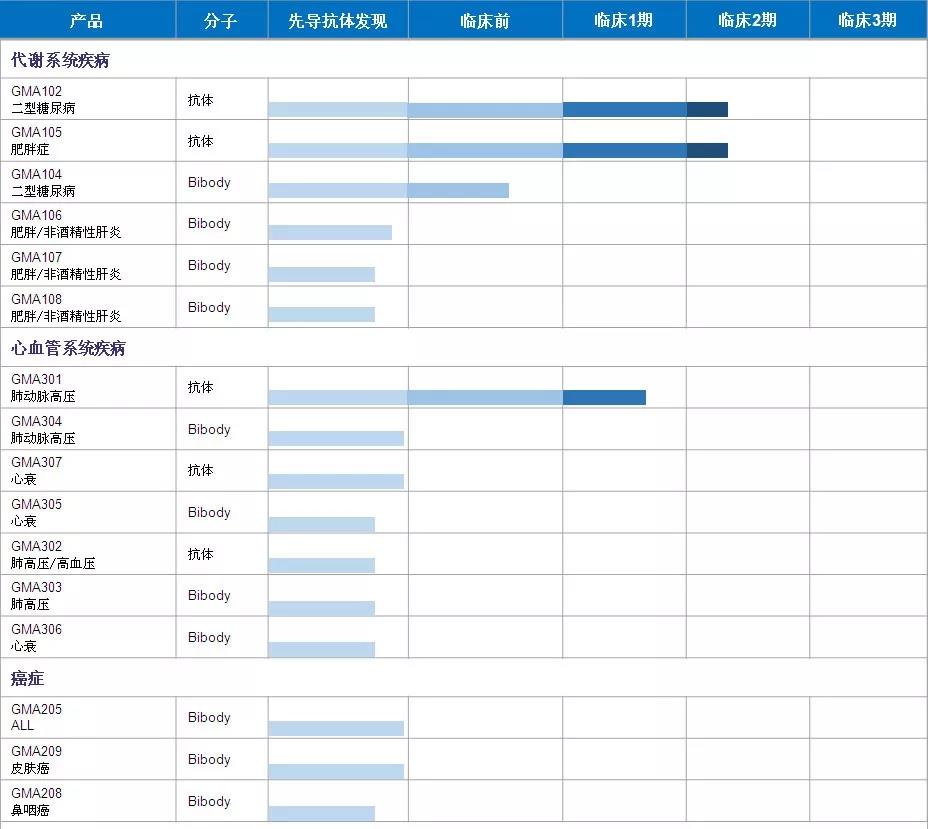
除此之外,鸿运华宁针对鼻咽癌、食道癌和其它几类癌症的多个抗体新药正在临床前开发过程中。根据该公司官网资料,该公司所有在研产品均属原创,目标定位于全球市场,并在中国和海外同步开展临床开发。
祝贺鸿运华宁肺动脉高压抗体药物在中国的临床申请获得临床默示许可,希望这款新药临床研究顺利,早日为患者带来更多治疗选择。





