中国国家药监局药品审评中心(CDE)网站最新数据显示,神州细胞已在中国提交了甲型血友病治疗药物重组人凝血因子VIII(SCT800)的上市申请。这不仅是神州细胞首个申报上市的产品,也是首个申报上市的国产重组人凝血因子VIII。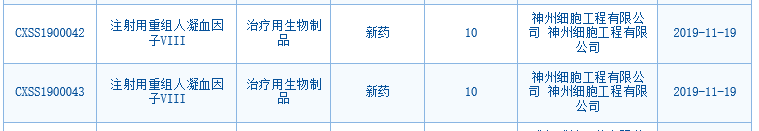
甲型血友病又称A型血友病,是一种遗传的终生性疾病,大部分患者从出生体内就缺少凝血因子Ⅷ,轻微地触碰就会出血,重症患者没有明显外伤也可发生“自发性”出血。目前在我国,血友病标准治疗率低,长期预后差而导致血友病儿童超过90%已出现不同程度的关节病变。SCT800为神州细胞自2008年开始自主研发的重组人凝血因子VIII蛋白,拟用于治疗甲型血友病。目前,神州细胞已经在成人及青少年甲型血友病中完成了SCT800的3期临床研究,同时正在进行SCT800对儿童、成人及青少年患者的预防治疗3期研究。神州细胞是一家领先的创新型生物制药研发公司,专注于恶性肿瘤、自身免疫性疾病、感染性疾病和遗传病等多个疾病治疗和预防领域的生物药产品研发和产业化。今年9月16日,神州细胞刚向上海证券交易所提交了科创板IPO申请。根据神州细胞的招股书,截至2019年7月31日,该公司的产品管线包括21个创新药和2个生物类似药,其中8个产品获准进入临床研究阶段,6个品种完成药性评价进入临床前研究阶段,9个品种完成候选药物开发进入性评价阶段。除了重组人凝血因子VIII SCT800外,神州细胞的其它研究进展较快的产品包括SCT200、SCT-I10A、SCT400等多款产品。SCT400是一款CD20单抗,其针对非霍奇金淋巴瘤的3期临床研究已经完成。SCT200产品为神州细胞自主研制的全人源EGFR单抗(IgG1亚型),其正在结直肠癌、头颈鳞癌、三阴乳腺癌等多种实体瘤中开展1期和2期临床研究。SCT-I10A为神州细胞研发的拟用于治疗多种实体瘤的重组人源化抗PD-1 IgG4型单克隆抗体,神州细胞已在实体瘤或淋巴瘤、头颈鳞癌中开展了三项关于SCT-I10A单药或联合疗法的临床研究。


