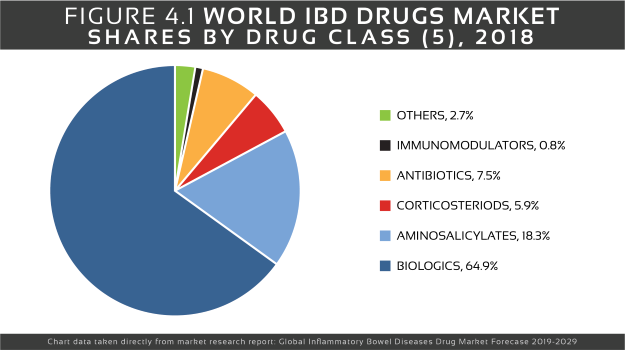
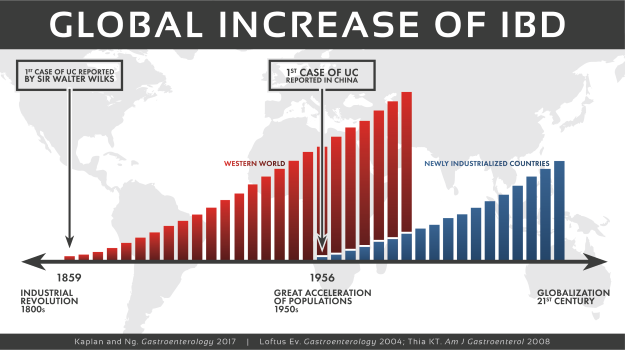
炎症性肠病(IBD)指以胃肠道慢性炎症为特征的疾病,最常见的是克罗恩病和溃疡性结肠炎。长期的慢性炎症会损害受影响的胃肠器官正常运作功能,导致持续性腹泻、腹痛、直肠出血、体重减轻和疲劳等症状。从历史上看,IBD主要见于工业化国家,北美和欧洲报告的患病率最高。单在美国,大约有160万人患有克罗恩病或溃疡性结肠炎,每年诊断的IBD新发病例多达7万例。尽管目前北美和欧洲的IBD发病率已趋于稳定或下降,但因患病率超过0.3%,负担仍然很重。此外,过去的30年里,IBD在非洲、亚洲和南美洲等新兴工业化国家的发病率有所上升。
图片来源:BioSpace
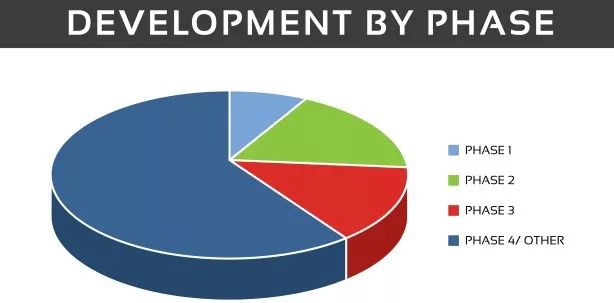
IBD的确切病因尚不完全清楚,但它涉及免疫系统、基因和环境因素之间的相互作用。在基因方面,有研究表明,5%−20%的受感染者有罹患其中一种疾病的一级亲属(父母、子女或兄弟姐妹)。许多与IBD相关的基因和基因突变已经被证实,其中包括NOD2/CARD15基因的突变。北美和欧洲高达20%的IBD患者可能有NOD2/CARD15基因突变。虽然基因检测是可行的,但它目前还不是IBD诊断过程的一部分,且基因检测只能识别出一个人患IBD的潜在风险,但不能预测IBD是否会发展。目前还没有治愈IBD的方法。现在治疗的目的主要是减少引发病症的炎症,从而提供短期或长期的缓解,降低并发症的风险。IBD的治疗通常包括药物治疗或手术。用于治疗IBD的药物包括抗炎药、免疫抑制剂、生物制剂和抗生素。抗炎药通常是治疗炎症性肠病的第一步,包括皮质类固醇和氨基水杨酸盐(5-ASA),如艾尔建的美沙拉秦、Salix Pharma公司的巴柳氮和布地奈德以及阿斯利康的Entocort EC。免疫抑制剂可以阻止肠壁释放炎症诱导化学物质的免疫反应。相关药物包括硫唑嘌呤(Azasan、Imuran)、巯嘌呤(Purinethol、Purixan)、环孢素(Gengraf、Neoral、 Sandimmune)和甲氨蝶呤(Otrexup、Rasuvo、Rheumatrex Dose Pack、Trexall、Xatmep)。生物制剂——肿瘤坏死因子(Tumor necrosis factor,TNF)-α抑制剂是一类抑制人体对TNF(由参与早期炎症事件的白血球细胞产生的蛋白质)自然反应的药物。例如艾伯维的Humira(阿达木单抗)、Janssen的Simponi(戈利木单抗)。其他常用的生物疗法有Tysabri(那他珠单抗)、Entyvio(维多珠单抗)和Stelara(乌司奴单抗)。抗生素可以与其他药物一起使用,或者当患者存在感染问题时使用。常用的抗生素包括环丙沙星(Cipro)和甲硝唑(Flagyl)。目前正在通过临床试验探索多种靶向治疗方法。除了TNF-α抑制剂、氨基水杨酸盐和糖皮质激素外,常见的靶点和机制包括:i. Janus激酶(JAK)3抑制剂。JAK通路被认为在炎症过程中起着重要作用,因为它们参与50多种细胞因子和生长因子的信号传导,其中许多细胞因子和生长因子驱动免疫介导的疾病。ii. 选择性S1P受体调节剂。S1P受体参与了包括自身免疫性疾病在内的多种生物应答的调节。iii. 人白细胞介素(IL)-12、IL-22、IL-23和IL-36抑制剂。IL是一类炎症细胞因子,是作为免疫系统的一部分参与炎症反应的一类蛋白质。iv. 二氢乳清酸脱氢酶(DHODH)抑制剂。DHODH抑制对活化的免疫细胞具有选择性的免疫调节作用。截至2019年10月,clinicaltrials.gov上列出了730项IBD相关临床试验(Recruiting、Not yetrecruiting、Active、notrecruiting、Enrolling by invitation Studies)。这些试验中,268项在美国展开,其余在全球各地进行。如果按阶段划分,Ⅰ期试验有63项,Ⅱ期试验有132项,Ⅲ期试验有101项,其余的是Ⅳ期或其他类型的研究。
图片来源:BioSpace
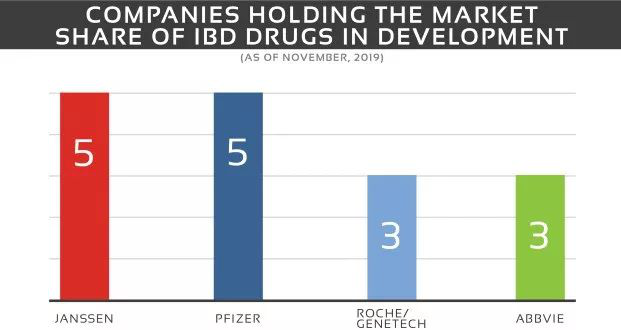
以下对选定的开发中药物的分析(并非全面)将简要讨论每种药物的作用机制以及临床试验阶段。截至2019年10月,该信息是最新的。IBD市场由不同规模的制药和生物技术公司组成。市场份额由Janssen主导,其在所有阶段(I-III期试验)拥有5种在研药物:戈利木单抗、乌司奴单抗、JNJ-64304500 (JNJ-4500/IPH-2301/NN-8555)、JNJ-67864238、古塞库单抗单一疗法及与戈利木单抗联合疗法。其他公司包括,辉瑞在I和II期试验有5种药物:PF-06687234、[124I]IB-PF-06687234、PF-06651600、PF-06700841:PF-06651600、PF-06480605。罗氏与基因泰克合作,在I-III期试验中有3种药物:UTTR1147A/RG7880、依曲利单抗(RG7413)、RO7049665。艾伯维在II期、II/III期和III期试验有3种药物:ABBV-323、Risankizumab(ABBV-066)、乌帕替尼(ABT-494)
图片来源:BioSpace
Aevi Genomics已经与Kyowa Kirin合作开发了AEVI-002,这是一种全人源单抗,它结合了一种在肠道组织中发现的被称为LIGHT的炎症蛋白。相关试验正在评估AEVI-002治疗儿童严重克罗恩病的疗效,初步数据预计在2019年下半年公布。Assembly Biosciences正在对轻度至中度活跃溃疡性结肠炎患者进行活体生物药(live biotherapeutic product,LBP)候选药物ABI-M201的Ib期临床试验。Assembly和Allergan已经开始合作,共同开发用于溃疡性结肠炎、克罗恩病和肠易激综合征的LBP化合物。ABI-M201是此次合作的第一个LBP候选药物。Enterome与武田合作,共同开发和商业化一个first-in-class、非全身性的口服小分子EB8018(TAK018)。EB8018可以阻断细菌表达细菌毒性因子FimH(肠道炎症级联反应的关键诱导因子),从而减少克罗恩病患者的肠道炎症。EB8018治疗克罗恩病的Ib期临床试验的初步数据预计在2019年完成。武田计划于2019年11月开始Ⅱ期试验。Gossamer Bio正在开发口服HIF-1α稳定剂GB004。今年第二季度开始进行活跃性轻度至中度溃疡性结肠炎Ib期研究的患者登记,公司预计2020年上半年公布研究的主要结果。OSE Immunotherapeutics具有一个针对免疫肿瘤和自身免疫性疾病的药物管线。OSE-127是这条管线中的药物之一,它是一种靶向CD127受体(IL-7受体的α链)的单克隆免疫调节抗体,对效应T淋巴细胞产生强烈的拮抗作用。IL-7受体的阻断阻止了致病性T淋巴细胞的迁移,同时保留了对自身免疫性疾病有积极影响的调节性T淋巴细胞。第一批患者于2018年12月进行了Ⅰ期试验。Bridge Biotherapeutics正在评估一种Pellino-1小分子抑制剂BBT-401。Pellino-1是一种连接酶,被视为多种免疫受体信号通路的关键介质。BBT-401在80名健康志愿者的I期研究中被证明具有良好的耐受性和安全性。此外,还有研究数据显示其没有或只有最少的全身暴露的关键特征。目前,一项随机、安慰剂对照、剂量递增的II期试验正在招募48名溃疡性结肠炎患者。百时美施贵宝的BMS-986165是一种口服、选择性酪氨酸激酶2(TYK2)抑制剂。TYK2是一种细胞内信号激酶,介导细胞因子驱动的免疫和促炎症信号通路,在免疫介导疾病的慢性炎症循环中起关键作用。2018年银屑病患者的II期试验成功完成。目前正在进行两个II期试验,克罗恩病和溃疡性结肠炎各一个。礼来公司正在研制mirikizumab(LY 3074828),这是一种人源化IgG4单抗,可结合并抑制IL-23的p19亚单位。克罗恩病患者II期SERENITY试验和溃疡性结肠炎II期试验均报告阳性结果。两项试验均表明,与安慰剂相比,mirikizumab治疗的患者在12周时获得的临床缓解率和内窥镜检查症状减轻率显著提高。礼来目前正在进行克罗恩病和溃疡性结肠炎的II期和Ⅲ期的临床试验。Gilead与Galapagos NV合作正在研究一种高度选择性JAK1抑制剂filgotinib。II期研究FITZROY的结果于2017年12月发表在《柳叶刀》上。本研究探讨了filgotinib治疗活跃性中重度克罗恩病的疗效和安全性。数据显示,与安慰剂相比,filgotinib治疗后临床缓解患者明显增多,且具有可接受的安全性。目前有7个正在进行的II期和Ⅲ期试验,包括MANTA、DIVERSITY、DIVERGENCE2和SELECTION1。Immunic Therapeutics正在开发一种可抑制二氢硼酸脱氢酶(DHODH)的小分子药物口服片剂。Immunic在2017年完成了两项Ⅰ期研究,评估了健康志愿者每天一次或重复使用IMU-838的剂量,研究结果支持每天重复给药高达50mg的IMU-838的耐受性。目前,Immunic的II期试验CALDOSE 1正在对溃疡性结肠炎进行研究。Seres Therapeutics的SER-287是一种使用Seres专有的微生物治疗平台开发的口服胶囊。它属于生物来源,包含一个活的和多种细菌孢子的联合体。SER-287被设计用来减少免疫激活的触发而非抑制免疫系统。溃疡性结肠炎患者的Ib期试验结果显示,SER-287微生物组治疗可提高临床缓解率和内窥镜诊断评分。II期试验ECO-RESET目前正在招募200名18−80岁患有活跃性轻度至中度溃疡性结肠炎的成年人。Sublimity Therapeutics利用Sublimity专有的SmPill®给药系统开发出一种口服环孢素制剂,称为ST-0529。与传统口服或静脉注射环孢素不同,SmPill®技术能够将环孢素准确地直接输送到结肠病变组织中,从而最大限度地减少全身暴露和不必要的副作用。在一项IIa阶段的研究中,ST-0529显示出良好的安全性和耐受性。一项IIb阶段的研究AURORA(CYC-202)目前正在招募280名中度至重度溃疡性结肠炎患者。Arena Pharmaceuticals正在开发etrasimod,这是一种新一代的口服高选择性1-磷酸鞘氨醇(S1P)受体调节剂,用于优化S1P受体1、4和5的药理学和作用,这可能会提高药物疗效和安全性。II期OASIS试验达到主要的和所有次要终点。基于这些结果,Arena启动了全球III期ELEVATE溃疡性结肠炎计划,该计划包括两项全球临床试验和一项开放标签扩展研究。此外,克罗恩病患者的II/III期试验也正在计划中。Celgene的ozanimod以S1P-1和-5受体为靶点。2017年10月报告了II期试验的结果。在II期STEPSTONE开放性研究中,ozanimod在第12周对中度至重度活动性克罗恩病患者的临床缓解和内窥镜检查结果显示出有意义的改善。Celgene目前正在对两种类型的IBD进行9项积极的研究。武田株式会社Shire的ontamalimab(SHP 647)进入III期开发阶段,SHP 647是一种针对粘膜定位蛋白细胞粘附分子(MADCAM1)的全人IgG2单抗。Shire于2016年从辉瑞获得了该药物的许可。2017年,《柳叶刀》杂志发表了溃疡性结肠炎患者的II期试验结果,证明这种疗法在该患者群体中安全且耐受性良好,在诱导缓解方面优于安慰剂。7个III期试验目前正在招募溃疡性结肠炎和克罗恩病患者。尽管IBD的治疗取得了显著进展,但目前的治疗方案仅使一部分患者得到缓解。根据 Gastroenterology & Hepatology 杂志2016年7月版发表的一篇文章,目前生物药治疗带来的缓解率约为20%至35%,约45%至60%的患者实现应答。相反,这意味着40%到55%的患者对治疗没有应答,65%到80%的患者没有得到完全缓解。此外,随着时间的推移,使用生物制剂治疗的患者可能会对治疗失去持久应答,从而导致症状复发。除了继续开发RNA小分子抑制剂和细胞内细胞因子途径(例如反义寡核苷酸疗法和JAK抑制剂)以及生物制剂(例如IL-12和IL-23抑制剂、单克隆抗体和S1P抑制剂)外,IBD的未来治疗还包括调整肠道微生物群,以及鉴定与IBD相关的基因组以开发个性化治疗。一篇发表在 Translational Pediatrics 杂志上题为《炎症性肠病的个性化药物现状和未来展望》的论文也回应了这一趋势。文章概述了IBD治疗模式转变的益处,讨论了IBD患者个性化治疗的潜力,并认为这是IBD患者管理策略上的一个重大进步,而不是继续传统的基于症状、结果和并发症的治疗方法。参考资料:
1# Inflammatory Bowel Disease Insight Report: Current Therapies, Drug Pipeline and Outlook (来源:BioSpace)