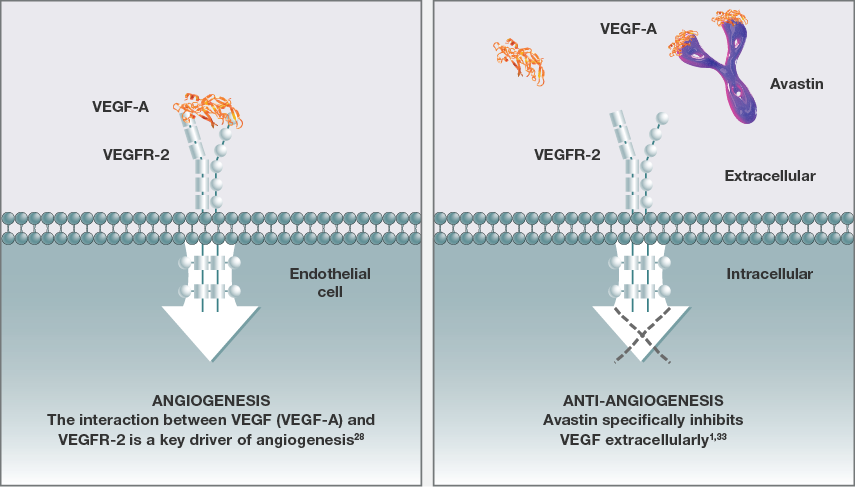
贝伐珠单抗的原研药物为罗氏(Roche)的安维汀(贝伐珠单抗),该药是一种人源化单克隆抗体IgG1,属血管内皮生长因子(VEGF)抑制剂。血管内皮生长因子(VEGF)是肿瘤血管生长中所必需的一种蛋白质,贝伐珠单抗通过与VEGF结合,抑制VEGF与其受体结合,阻断血管生成的信号传导途径,抑制肿瘤细胞生长。自2004年在美国获批上市以来,贝伐珠单抗已在全球范围内获批囊获转移性结直肠癌、乳腺癌、宫颈癌、卵巢癌、非小细肺癌等多种适应症。

在中国,罗氏安维汀(贝伐珠单抗)已获批转移性结直肠癌、非鳞状细胞非小细胞肺癌适应症。2019年12月,齐鲁制药研制的安可达(贝伐珠单抗生物类似药)获中国国家药品监督管理局(NMPA)批准上市,治疗晚期、转移性或复发性非小细胞肺癌、转移性结直肠癌患者,是首个在中国获批的贝伐珠单抗生物类似药。
Mvasi是安进公司和艾尔建公司联合开发的贝伐珠单抗生物类似药,该药最早与2017年9月获得美国FDA批准治疗转移性结直肠癌、非小细胞肺癌、胶质母细胞瘤、肾细胞癌、宫颈癌五种癌症,随后又于2018年1月获欧盟批准治疗转移性结直肠癌、转移性乳腺癌、非小细胞肺癌、肾细胞癌等多种癌症,是美国FDA和欧盟批准的首个贝伐珠单抗生物类似药。
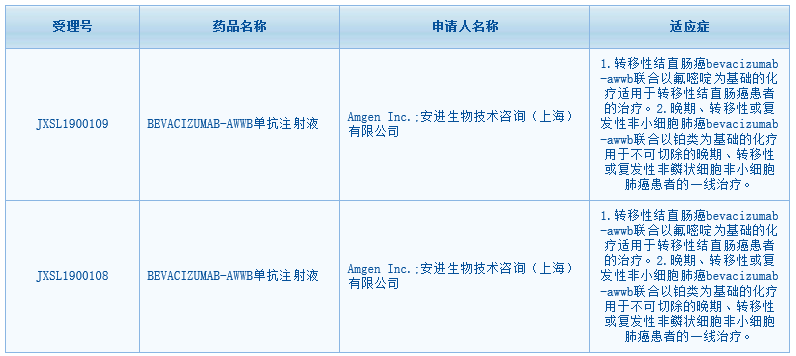
本次在中国,Mvasi获批两项临床试验:一项是联合以氟嘧啶为基础的化疗适用于转移性结直肠癌患者的治疗;另一项是联合以铂类为基础的化疗用于不可切除的晚期、转移性或复发性非鳞状细胞非小细胞肺癌患者的一线治疗。
我们祝贺Mvasi(bevacizumab-awwb)在中国获批临床,希望其临床研究顺利开展并取得好的结果,早日为患者带来更多的治疗选择。

