作为全球首个获批用于治疗系统性红斑狼疮的生物制剂,注射用贝利尤单抗(belimumab)在中国的注册再获新进展。4月14日,中国国家药监局药品审评中心(CDE)最新公示,葛兰素史克(GSK)旗下注射用贝利尤单抗的上市申请拟纳入优先审评(受理号为JXSS2000003/4),理由是“儿童用药纳入优先审评”。这意味着,儿童红斑狼疮首款创新疗法有望加速在中国获批上市。
贝利尤单抗是一种重组的完全人源化IgG2λ单克隆抗体,通过抑制B细胞的增殖及分化,诱导自身反应性B细胞凋亡,从而减少血清中的自身抗体,达到治疗系统性红斑狼疮的目的。早在2011年3月,贝利尤单抗(海外商品名:Benlysta)就得到了美国FDA的批准。至2019年4月,该药物再次获得FDA批准,用于治疗患有系统性红斑狼疮(SLE)的儿童患者,成为FDA批准的首款能够治疗儿童红斑狼疮患者的创新疗法。
据悉,这款疗法治疗儿童患者的潜力在临床试验中得到了验证。在一项研究里,93名罹患系统性红斑狼疮的儿童患者接受了长达52周的Benlysta静脉输注治疗。研究人员们发现,相比接受安慰剂 + 标准疗法的儿童患者,接受Benlysta + 标准疗法的患者中,有更高比例达到了SLE缓解指数(SRI-4),即本研究的临床终点。而且,治疗组的儿童出现严重爆发(severe flare)的风险更低,两次爆发之间的间隔时间也更长。

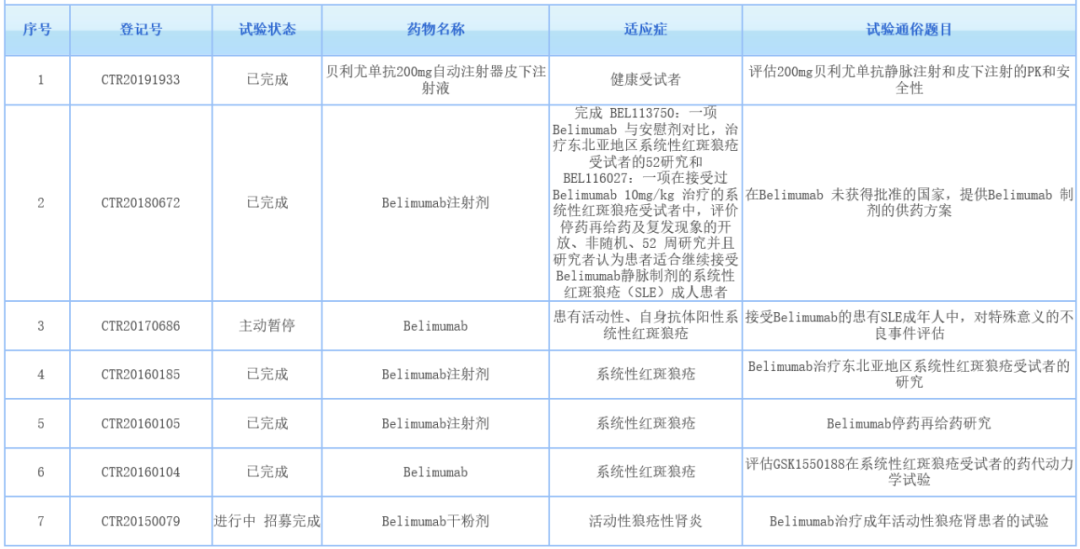
在安全性上,儿童患者体内的药物动力学数据与成人中获得的数据一致,最常见的副作用包括恶心、腹泻、以及发烧。需要注意的是,患者经常会出现输注反应,因此FDA建议在治疗前,医生为患者明确治疗风险,并提供抗组胺剂。在中国,注射用贝利尤单抗于2019年7月通过优先审评在中国获批,用于正在接受标准治疗的活动性、自身抗体阳性的系统性红斑狼疮(SLE)成人患者,商品名为倍力腾。根据中国药物临床登记与信息公示平台数据,目前在中国开展的贝利尤单抗的多项临床研究已经完成。
系统性红斑狼疮是一种自身免疫性疾病,目前还无法治愈。伴随疾病的发展,患者会出现关节疼痛或肿胀、极度疲劳、无法解释的发热、皮肤起皮疹、以及器官受损等多种症状。尽管罹患系统性红斑狼疮的儿童患者并不多见,其病情发展却比成人患者要来得更为猛烈。相比成年患者,儿童患者的肾脏和中枢神经系统会更容易受到侵害,他们因此出现严重器官损伤和并发症的风险也来得更高。目前,儿童红斑狼疮患者的治疗方案非常有限。
随着GSK公司该款药物被CDE拟纳入优先审评,意味着该药物在中国用于治疗儿童红斑狼疮的上市申请有望获得加速批准。希望这款药物早日给更多儿童红斑狼疮患者带来新的治疗选择。





