mRNA疫苗,是将编码抗原蛋白的mRNA直接导入到人体细胞内,通过人体细胞的翻译系统合成相应的抗原蛋白,进而诱导人体产生对该抗原蛋白的免疫应答,以达到预防病毒感染或治疗疾病的目的。
mRNA疫苗,将体外的表达过程转移到体内,能够大大缩短了研发时间,降低研发成本,是对传统疫苗和药物研发的一次技术革新。在mRNA疫苗成功应用于新冠肺炎之前,全世界的科学家已经在研究mRNA疫苗在癌症预防和治疗中的用途,但始终未获得突破性进展。

中国国家纳米科学技术中心(NCNST)的科学家在《Nano Letters》上发表了题为“In Situ Transforming RNA Nanovaccines from Polyethylenimine Functionalized Graphene Oxide Hydrogel for Durable Cancer Immunotherapy”论文,报道了其设计的一种水凝胶,可提供带有免疫刺激佐剂的mRNA疫苗。
研究团队设计了一种包含氧化石墨烯(RO)和低分子量聚乙烯亚胺(LPEI)的水凝胶,可用于递送携带了免疫刺激佐剂的mRNA疫苗,氧化石墨烯具有表面积大的特点,可以有效载药,而聚乙烯亚胺则能够结合mRNA进行翻译。将这种疫苗注射到黑色素瘤小鼠体内后,其活性至少可以维持30天,抑制肿瘤生长并防止转移。
结果表明水凝胶输送系统具有潜力,可以帮助mRNA疫苗实现长期的抗肿瘤作用,如癌症免疫疗法。研究人员还添加了Galderma公司开发的TLR7/8激动剂瑞喹莫德(Resiquimod)作为佐剂,进一步增强对抗肿瘤免疫反应至关重要的抗原特异性CD8+T细胞的刺激和扩增。
在癌症中,疫苗通常被设计为翻译与肿瘤相关的抗原,因此免疫系统可以识别并消除癌症。短暂的免疫过程可以预防COVID-19,但是在癌症治疗中,需要更持久的mRNA递送才能达到稳定的治疗效果。
为了测试其mRNA平台,研究人员使用卵清蛋白(一种在鸡蛋白中发现的蛋白)作为模型抗原。他们将卵清蛋白mRNA和佐剂与水凝胶混合,并将其注射到黑素瘤肿瘤小鼠的皮肤下,该瘤被设计为在其表面表达卵白蛋白。
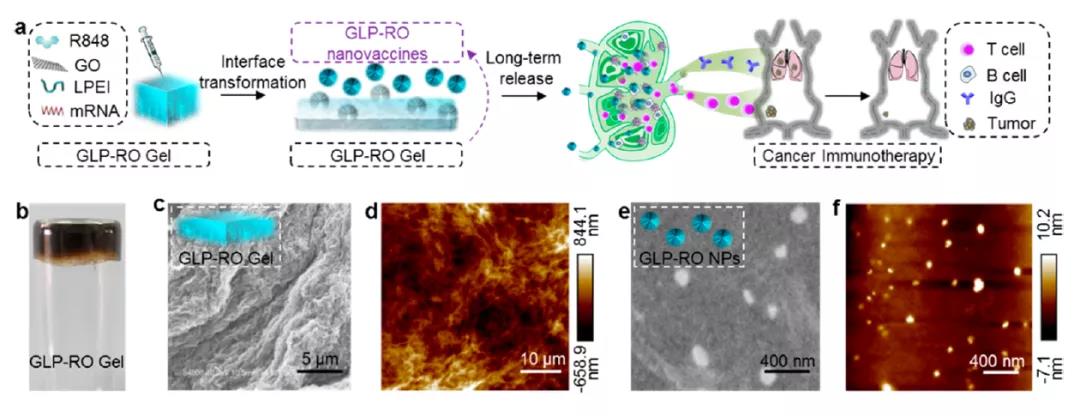
研究小组显示,水凝胶至少在30天之内稳定地将疫苗(包括mRNA和佐剂)释放到纳米颗粒中,并迁移到淋巴结。
与接受游离佐剂和无水凝胶mRNA的小鼠或接受无佐剂mRNA水凝胶的小鼠相比,仅接受一次完整疗法注射的动物的肿瘤明显较小。科学家发现,接受了完整疗法的小鼠也显示出进入肿瘤的CD8+ T细胞数量最多。
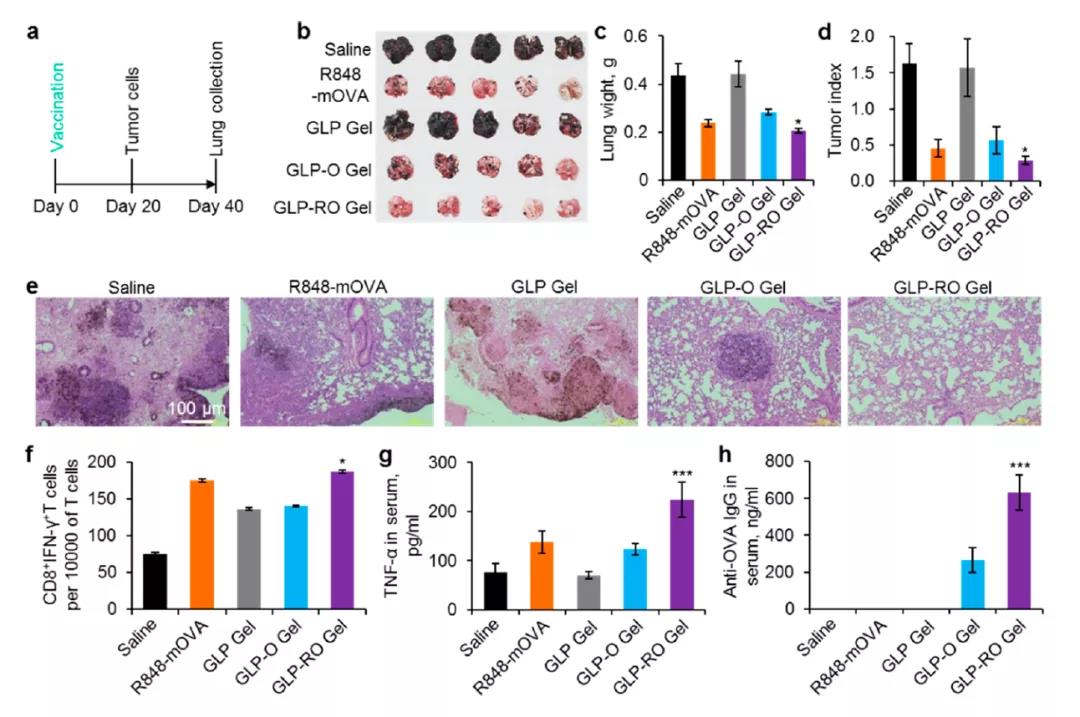
而且,与其他抗体相比,新型的mRNA凝胶疗法在血清中诱导了最高水平的卵白蛋白特异性抗体,表明它不仅抑制了肿瘤的生长,而且还防止了肿瘤的复发或形成远处转移。
该研究提示,氧化石墨烯-聚乙烯亚胺水凝胶递送mRNA+佐剂,能够实现持久的癌症免疫治疗效果,有望成为有效的癌症mRNA疫苗递送平台。

