Cybrexa Therapeutics今日宣布,临床前癌症模型证明,在研肽偶联药物(PDC)CBX-12能增强免疫检查点抑制剂的效果。目前,Cybrexa正在进行一项1/2期临床试验,以确定CBX-12的耐受性和安全性。该公司的初步重点将针对HER2过度表达的卵巢癌和小细胞肺癌(SCLC)患者。
免疫检查点抑制剂与化疗联用是多种实体瘤的标准疗法,但与化疗相关的骨髓抑制会降低免疫疗法的疗效。并且,由于其对正常细胞的影响,化疗还会产生各种毒副作用。而靶向化疗,如抗体偶联药物(ADC)则受限于只能治疗表达高水平靶抗原的肿瘤。那么,有没有什么办法,既能特异性地靶向广泛的肿瘤类型,又能避免毒性呢?所有肿瘤的特征之一就是酸性微环境。而CBX-12可将一种强效的细胞毒素exatecan,特异性递送至低pH值环境的细胞中。它利用了一种低pH插入肽(pHLIP)的独特变体,低pH值改变这种多肽的构象,将exatecan递送至细胞内。这种选择性靶向肿瘤细胞的作用机制,避免了与疗法攻击健康细胞相关的毒性。临床前癌症模型显示,CBX-12不会像化疗一样诱导骨髓抑制。
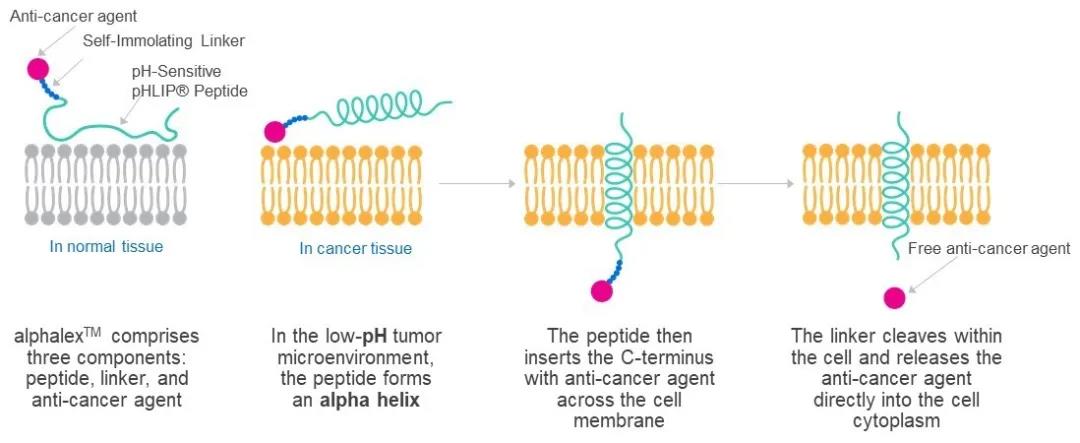
▲利用低pH插入肽将抗癌药物递送到肿瘤细胞的机制(图片来源:Cybrexa公司官网)研究人员使用结直肠癌小鼠模型,进一步评估了CBX-12对PD-1和CTLA4免疫检查点抑制剂疗效的影响。实验结果显示,与单独使用免疫检查点抑制剂的小鼠相比,接受联合疗法治疗的小鼠肿瘤生长显著延缓,存活率提高,并表现出完全的肿瘤消退。具体而言,CBX-12与PD-1抑制剂联用延缓小鼠肿瘤生长4倍,与CTLA4抑制剂联用延缓肿瘤生长10倍。不仅如此,经历肿瘤完全消退的小鼠还表现出长期的免疫记忆。而将CBX-12处理的肿瘤细胞注射到小鼠体内,可导致抗肿瘤免疫应答,表明CBX-12诱导了免疫原性细胞死亡。“抗体偶联药物受限于肿瘤需要表达高水平的靶抗原。而CBX-12的新颖之处在于它靶向酸性环境,这是所有肿瘤的普遍特征。因此,我们能够在更广泛的患者群体中,选择性地将一种强效抗癌药物递送至肿瘤细胞。”Cybrexa的生物学副主任Sophia Gayle博士表示,“我们的研究结果表明,将CBX-12与免疫检查点抑制结合,可以将免疫疗法的疗效扩展到正常情况下对它们不产生应答的肿瘤。考虑到约80%的患者对免疫检查点抑制剂单药治疗没有反应,这可以使广泛的患者受益。Gayle博士也指出,由于实验都在临床前模型中进行,未来还需要进行额外的研究以了解这种组合疗法对患者的影响。



