2021年10月10日,4D Molecular Therapeutics(4DMT)宣布,其玻璃体内注射基因疗法4D-125,在治疗晚期X连锁视网膜色素变性(XLRP)患者的1/2期临床试验中,取得积极的中期安全性和临床活性数据。

X连锁视网膜色素变性是一种进展缓慢的遗传性视网膜营养不良疾病,由RPGR基因突变引起,可导致视力丧失乃至失明。目前患者没有可用的治疗选择。4DMT的发现平台称为“Therapeutic Vector Evolution”,可以从包含10亿个不同腺相关病毒(AAV)衣壳蛋白的文库中筛选出为特定疾病“量体裁衣”的AAV载体衣壳。它们不但具有更高的组织特异性,而且不会受到患者体内中和抗体的影响,在递送基因方面也更为安全。4D-125使用的正是该平台开发的R100 AAV载体,能靶向视网膜感光细胞特异性地递送PRGR基因。与其他在研基因疗法不同,4D-125只需在玻璃体内注射,就可以将转基因递送到视网膜的整个表面,比起视网膜下给药可潜在治疗更广泛的患者群体。
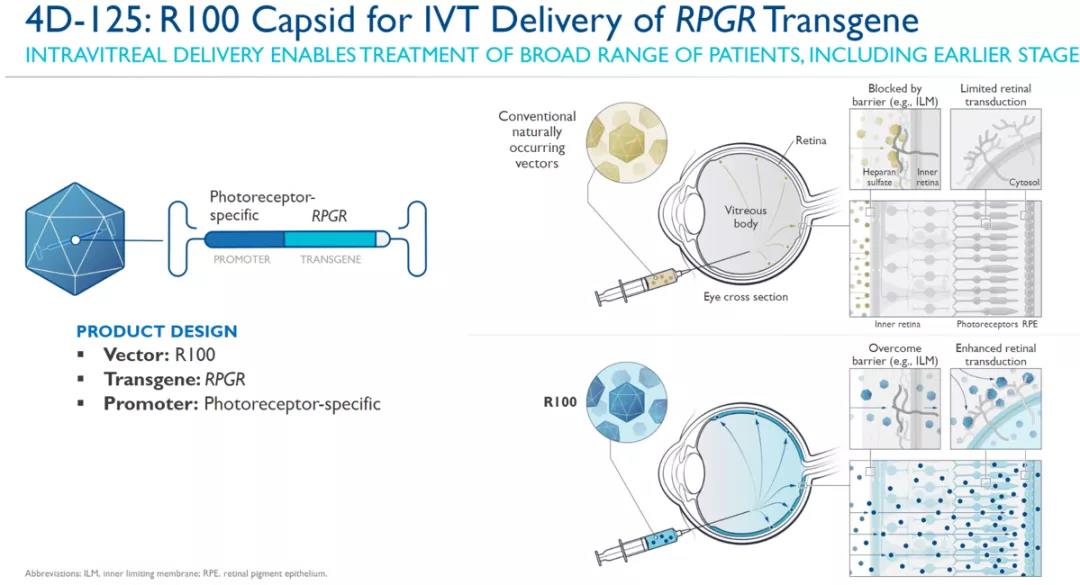
▲4D-125作用机制(图片来源:参考资料[2])截至2021年9月1日,该项正在进行的剂量递增和剂量扩增1/2期临床试验,已入组8例因RPGR基因突变导致晚期X连锁视网膜色素变性的患者。中期临床数据表明,4D-125耐受性良好,有望既能减缓患者视网膜感光细胞的损失,又可增强视网膜的敏感性。
- 4D-125在所有8例患者中均耐受良好,包括5例接受1E12 vg/眼最高剂量水平给药的患者。
- 未观察到剂量限制性毒性或严重不良事件。未观察到慢性炎症。
- 2例可评估疗效患者的数据均表明,在至少6个月随访时,与同一患者未接受治疗的对照眼相比,接受治疗眼的感光细胞得以更好的保存。并且,通过微视野检测(microperimetry),2名患者治疗眼平均视网膜敏感度获得改善,敏感度提高≥7 dB的位点数量比对照眼更多。
- 根据中期数据,研究人员计划继续在剂量扩展队列中,以1E12 vg/眼的最高剂量水平招募患者,包括较早期疾病患者。4DMT认为早期患者人群可能比晚期患者更有可能从该基因疗法中获益。
4DMT联合创始人兼首席执行官David Kirn博士表示:“这些数据支持了我们的观点,即4D-125耐受性良好,并且在单次玻璃体内注射后,有可能既能减缓患者感光细胞的进行性丧失,又能改善视觉功能。我们相信这些结果验证了我们Therapeutic Vector Evolution平台以及R100载体的潜力。”



