新一代心肌肌球蛋白抑制剂 aficamten 治疗肥厚型心肌病(HCM)中国一期临床研究完成;
Aficamten 在梗阻性肥厚型心肌病(oHCM)二期临床研究 REDWOOD-HCM 中结果积极;
为评价 aficamten 在 oHCM 患者中的作用,全球三期 SEQUOIA-HCM 临床研究将于 2022 年初启动,箕星药业主导其中的中国队列研究。
肥厚型心肌病(HCM)是最常见的遗传性心血管疾病,文献表明中国有超过 150 万 HCM 患者[1,2]。HCM 可导致劳力性呼吸困难、疲劳、胸痛、晕厥 / 先兆晕厥和运动能力受限[2]。与疾病相关的死亡率大多可归因于心源性猝死、心力衰竭和栓塞性卒中。HCM 是青少年和运动员猝死的主要原因之一,心脏性猝死常见于 10~35 岁的年轻患者,心力衰竭死亡多发生于中年患者,HCM 相关的心房颤动导致的卒中则以老年患者多见;总体而言,在三级医疗中心就诊的 HCM 患者年死亡率为 2%~4%[2]。因此 HCM 是一种严重危及患者生命,严重影响患者生存质量的疾病。[3]
目前指南推荐的 HCM 治疗药物主要包括 β 受体阻滞剂、维拉帕米、地尔硫卓和丙吡胺。对于那些无论静息还是激发时 LVOT-G ≥ 50 mmHg,伴有严重症状且药物治疗无效的梗阻性肥厚型心肌病(oHCM)患者还可以应用室间隔消减治疗(室间隔心肌切除术和经皮室间隔酒精消融术),但室间隔消减治疗应在有 HCM 多学科管理专家团队及相关治疗经验的医疗中心进行,并且由有经验的医师实施手术。总之,目前可用的治疗方法还不能完全满足 HCM 患者的治疗需求。[1~3]
Aficamten 是一种由 Cytokinetics 公司(美国加州)研发的新一代心肌肌球蛋白变构抑制剂, 可通过直接结合心肌肌球蛋白马达结构域和抑制肌球蛋白 ATP 酶,使马达处于稳定的非产力状态,从而减少每个心动周期中活性肌球蛋白产力横桥的数量,以降低心肌过度收缩。Aficamten 的作用机制提示其通过全面的化学优化来改善药物治疗指数和药代动力学特征,可能在心肌过度收缩的疾病如肥厚型心肌病的治疗中有效。
[4]
箕星药业于近日宣布顺利完成 aficamten 中国一期临床研究。该研究是一项在中国健康受试者中进行的,以评价 aficamten 的安全性、耐受性和药代动力学参数的双盲、随机、安慰剂对照、一期临床研究。实际研究中,共 28 例受试者随机分配并全部完成研究。总体展现了 aficamten 和安慰剂相似的良好耐受性以及与剂量成比例的药代动力学特性,这与先前在美国健康高加索人受试者中进行的一期临床研究观察到的结果相似。[4]
2020 年 7 月,箕星药业与 Cytokinetics 公司签订许可合作协议。根据协议,Cytokinetics 授予箕星在大中华区开发和商业化 aficamten (之前被称作 CK-274)的独家许可。箕星于 2020 年 9 月向国家药品监督管理局提交了 aficamten 片剂治疗梗阻性肥厚型心肌病新药临床试验申请,并在 2020 年 12 月获得批准。随着 aficamten 在中国一期临床研究的成功完成,箕星将与 Cytokinetics 合作开展 SEQUOIA-HCM 临床试验并主导中国队列研究。SEQUOIA-HCM 是 aficamten 在 oHCM 患者中的三期临床试验,由箕星开展其在中国的研究,Cytokinetics 将开展在中国之外的研究。
REDWOOD-HCM 研究是 Cytokinetics 针对有 oHCM 症状患者开展的二期多中心临床研究,并为 SEQUOIA-HCM 研究设计提供了依据。在前两个已经完成的研究队列中,患者以随机、安慰剂对照、双盲方式入组,旨在接受标准治疗药物的有 oHCM 症状的患者中进行剂量探索。第 3 个正在进行的队列以开放方式入组患者,以评估 aficamten 在包括丙吡胺的标准背景治疗基础上的作用。
本研究的主要目的是评估 aficamten 在有 oHCM 症状的患者中的安全性和耐受性。总体而言,REDWOOD-HCM 研究中 aficamten 治疗耐受性良好,治疗组间不良事件的发生率相似,未发生导致治疗中断或停药的用药后不良事件,也未发生被研究者归因于 aficamten 的严重不良事件。
本研究的次要目的是评价 aficamten 治疗 10 周后以超声心动评估的静息和 Valsalva 术后 LVOT-G 的浓度-效应关系。较安慰剂组,服用 aficamten 后,Valsalva 术后平均 LVOT-G 比基线有统计学意义的显著降低。绝大部分服用 aficamten 的患者达到了治疗目标,定义为在第 10 周时静息 LVOT-G < 30 mmHg 且 Valsalva 术后 LVOT-G < 50 mmHg (组 1 为 78.6%,组 2 为 92.9%;安慰剂组为 7.7% )。LVOT-G 在 aficamten 开始治疗 2 周内即出现降低,最大降低发生在开始剂量滴定 2 至 6 周并持续至治疗结束第 10 周。观察到的 LVOT-G 降低呈现剂量依赖,即随着 aficamten 剂量增加 LVOT-G 下降。
REDWOOD-HCM 队列 1 和队列 2 静息 LVOT-G (图片来源:Cytokinetics )
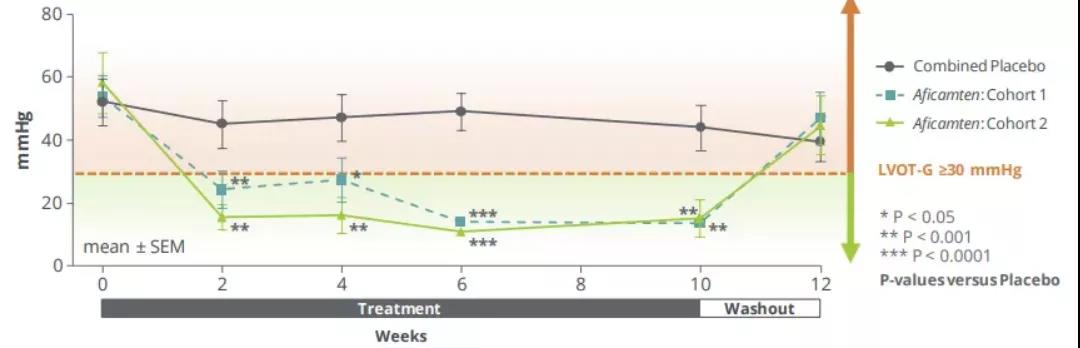
REDWOOD-HCM 队列 1 和队列 2 Valsalva 动作后 LVOT-G (图片来源:Cytokinetics )

SEQUOIA-HCM 是一项在有 oHCM 症状的患者中进行的随机、安慰剂对照、多中心双盲的三期临床研究。约 270 例合格患者将以 1:1 的比例随机接受 aficamten 或安慰剂治疗 24 周。使用超声心动图指导剂量滴定,以递增方式给予 5、10、15 或 20 mg aficamten 或匹配剂量的安慰剂。
SEQUOIA-HCM 的研究目标是给病人制定灵活的给药剂量从而个性化和最大化 aficamten 的治疗效应。
SEQUOIA-HCM 研究主要目的是通过从基线至第 24 周心肺运动试验(CPET)确定的最大摄氧量(pVO2)变化以评价 aficamten 的效应。次要目的包括从基线至第 12 周和第 24 周堪萨斯城心肌病调查问卷-临床综合评分(KCCQ-CSS)的变化,纽约心脏协会(NYHA)心功能分级改善 ≥ 1 级的患者比例,Valsalva 术后左室流出道压力阶差(LVOT-G)的变化,Valsalva 术后 LVOT-G < 30 mmHg 的患者比例以及心肺运动测试(CPET)期间总工作负荷的变化。SEQUOIA-HCM 研究预计在 2022 年初启动。
「在中国每天有将近 100 个人死于 HCM。基于临床前和临床数据,我们相信aficamten能对HCM病人产生有意义的影响。」箕星药业首席执行官罗万里(Joseph Romanelli)先生表示,「我们感谢参与一期临床研究的医生和健康受试者,同时我们期待在 2022 年与 Cytokinetics 合作开展全球三期 SEQUOIA-HCM 临床研究并主导其中的中国队列。」
参考文献
[1]. 中国医师协会心力衰竭专业委员会, 中华心力衰竭和心肌病杂志编辑委员会. 中国肥厚型心肌病管理指南2017. 中华心力衰竭和心肌病杂志. 2017; 1(2): 65-86.
[2]. 中华医学会心血管病学分会中国成人肥厚型心肌病诊断与治疗指南编写组, 中华心血管病杂志编辑委员会. 中国成人肥厚型心肌病诊断与治疗指南. 中华心血管病杂志. 2017;45(12): 1015-1031.
[3]. Ommen SR et al. 2020 AHA/ACC Guideline for the Diagnosis and Treatment of Patients With Hypertrophic Cardiomyopathy. Circulation. 2020 Dec 22;142(25):e533-e557.
[4]. 箕星官网链接:https://www.jixingbio.com/en/pipeline/
[5]. https://ir.cytokinetics.com/static-files/064f9a43-4e59-467d-a81c-51795f0cdf44
文章来源:药渡

