近日,STAT发布的一篇报告中对2022年第一季度值得关注的重要里程碑事件进行了盘点,其中包括关键临床试验的结果汇报和潜在美国FDA批准。在今天的这篇文章中,我们来看一看这些可能对新药开发进程产生重要影响的里程碑事件。Intellia Therapeutics/再生元:NTLA-2001去年,Intellia Therapeutics和再生元公司联合开发的体内CRISPR基因编辑疗法NTLA-2001的首个临床试验结果是CRISPR基因编辑领域的里程碑事件。NTLA-2001不但表现出良好的安全性,而且单剂NTLA-2001导致血清中的转甲状腺素蛋白水平(TTR)平均下降87%,在第28天TTR降低幅度最大可达96%。今年第一季度,该公司将汇报NTLA-2001治疗转甲状腺素蛋白淀粉样变性患者的1期临床试验的更多结果。

Nektar Therapeutics/百时美施贵宝:IL-2免疫刺激疗法/Opdivo组合
据统计,超过4000个临床试验在尝试不同在研疗法与抗PD-1/PD-L1抗体构成的组合疗法治疗癌症患者的功效。其中,Nektar Therapeutics的长效IL-2免疫刺激疗法bempegaldesleukin(简称bempeg)是一款倾向与IL-2信号通路中的CD122受体相结合的激动剂。它希望通过选择性激活IL-2信号通路,刺激CD8+效应T细胞,天然杀伤细胞和CD4+辅助T细胞的增殖。
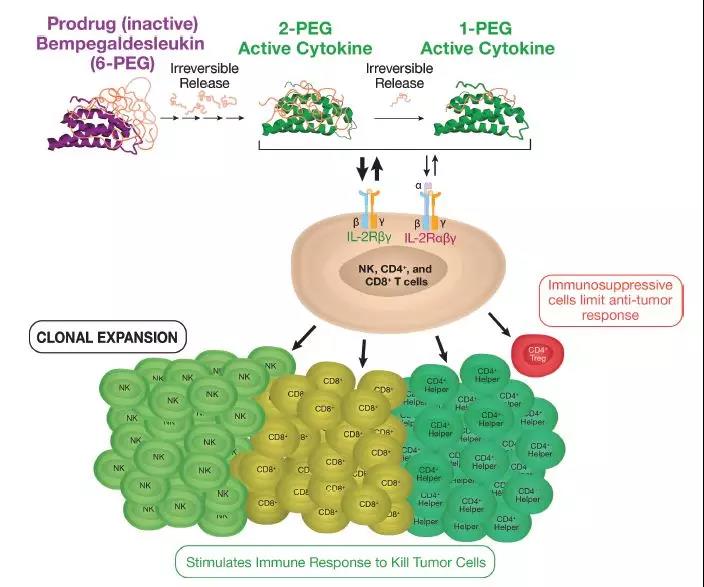
▲Bempegaldesleukin作用机制(图片来源:Nektar公司官网)
目前,bempegaldesleukin和抗PD-1抗体Opdivo构成的组合疗法在5项具有注册性潜力的临床试验中接受检验,其中一线治疗黑色素瘤和膀胱癌的临床试验有望在今年第一或第二季度获得结果。

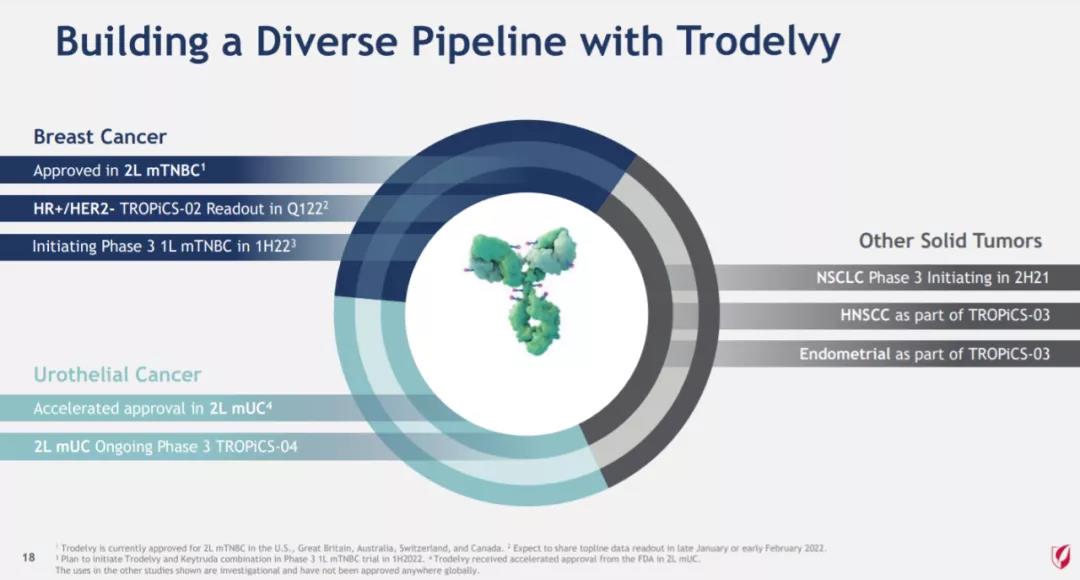
艾伯维公司正在开发一款治疗囊性纤维化的鸡尾酒疗法,由一款CFTR蛋白增强剂和两款CFTR蛋白调节剂组合而成。这款组合疗法的两项2期临床试验有望在第一季度获得结果,为这款疗法的疗效和安全性提供更为清晰的线索。去年,吉利德科学(Gilead Sciences)以约210亿美元收购Immunomedics,获得了靶向TROP2的“first-in-class”抗体偶联药物(ADC)Trodelvy(sacituzumab govitecan-hziy)。目前,它已经获得美国FDA的批准,二线治疗三阴性乳腺癌,以及经治膀胱癌患者。今年第一季度,Trodelvy治疗HR阳性/HER2阴性乳腺癌患者的3期临床试验将获得结果。积极数据有望进一步扩展Trodelvy可以造福的患者群体。Trodelvy是吉利德癌症研发管线中的基石性产品之一,目前还在多项临床试验中用于治疗非小细胞肺癌(NSCLC),头颈癌等癌症类型。
Springworks Therapeutics:nirogacestatNirogacestat是一款口服特异性γ-分泌酶小分子抑制剂。γ-分泌酶能够切割多种跨膜蛋白复合体,其中包括Notch蛋白。而Notch蛋白被认为能够激活导致硬纤维瘤生长的信号通路。
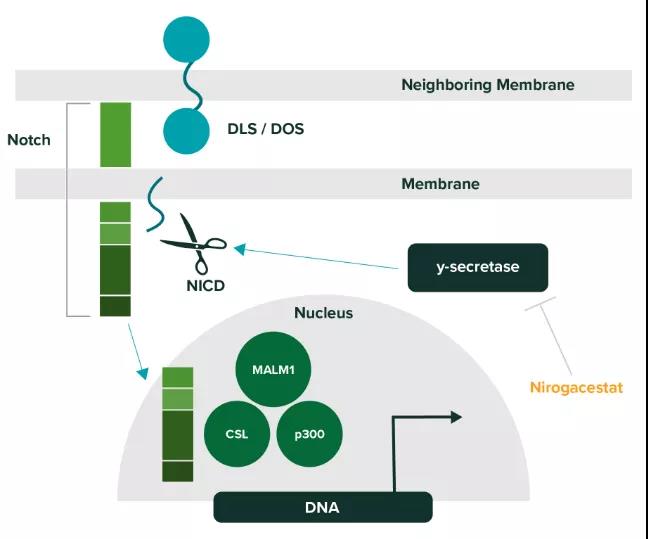
▲Nirogacestat的作用机制(图片来源:SpringWorks公司官网)
Nirogascestat在治疗包含24名硬纤维瘤患者的1期和2期临床试验中表现出100%的疾病控制率。它已经获得美国FDA授予的突破性疗法认定,用于治疗复发或难治性,无法切除的硬纤维瘤或深部纤维瘤病(deep fibromatosis)。Nirogascestat治疗硬纤维瘤患者的3期临床试验已经完成患者注册,预计在今年初获得结果。Sage Therapeutics/渤健:zuranoloneZuranolone是一款新一代γ-氨基丁酸(GABAA)受体别构调节剂。去年6月,Sage Therapeutics/渤健联合宣布,它在治疗重度抑郁症(MDD)患者的3期临床试验WATERFALL中达到主要终点,在第15天时显著改善患者的抑郁症状。今年第一季度,另一项名为CORAL的3期临床试验将获得结果。这项试验旨在检验zuranolone快速缓解MDD患者症状的效果。这些试验是支持zuranolone递交监管申请的临床开发项目的一部分。Madrigal Pharmaceuticals:resmetirom(MGL-3196)Resmetirom是一款潜在“first-in-class” 靶向肝脏的甲状腺激素受体(THR)β的口服选择性激动剂。甲状腺激素通过激活其β受体,在控制脂质代谢中发挥核心作用,影响人体的多个健康参数,从胆固醇和甘油三酯水平到肝脏中脂肪的病理累积。Resmetirom在治疗非酒精性脂肪性肝炎(NASH)患者的2期临床试验中已经表现出积极的活性。它的注册性3期临床试验有望在第一季度公布结果。
Intercept Pharmaceuticals:奥贝胆酸Intercept公司的奥贝胆酸也是一款治疗NASH的在研疗法。目前它在两项3期临床试验中接受检验。该公司指出,名为REVERSE的3期临床试验是目前唯一在因为NASH出现代偿性肝硬化的患者中进行的3期临床试验。这一试验结果有望在今年第一季度公布。Sierra Oncology:momelotinibMomelotinib是一款强力的选择性口服JAK1、JAK2和ACVR1抑制剂。两项已经完成的3期临床试验和其它2期临床试验表明,该药物在治疗骨髓纤维化时,具有与众不同的治疗特征:包括一系列对贫血状态有意义的改善,消除或减少频繁输血的需求,以及实现实质性控制脾脏和全身症状。
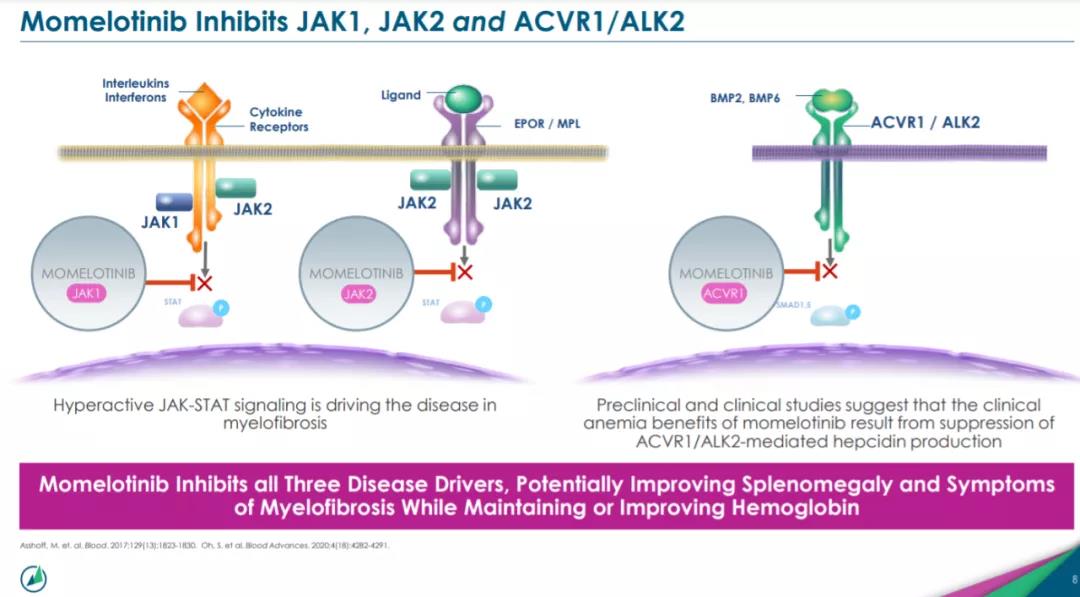
▲Momelotinib的作用机制(图片来源:Sierra Oncology公司官网)
Momelotinib用于治疗骨髓纤维化患者的关键性3期临床试验预计在今年2月获得顶线结果。ProQR Therapeutics:sepofarsenSepofarsen是一款反义寡核苷酸疗法,它是一种短链RNA分子,通过与CEP290基因表达的mRNA前体结合,恢复mRNA的正常剪接,从而增加眼睛感光细胞中CEP290蛋白的表达。CEP290蛋白的缺失是导致Leber先天性黑蒙症10(LCA10)的主要原因。在1/2期临床试验中,sepofarsen已经表现出可喜的活性。一名患者在接受了单次实验性RNA的治疗后,获得了长达一年以上的视力改善。这一创新疗法的关键性2/3期临床试验预计在今年第一季度末或第二季度初获得结果。此外,美国FDA可能在第一季度对以下多款创新疗法的监管申请做出回复:Agios Pharmaceuticals的潜在“first-in-class”口服丙酮酸激酶-R(PKR)别构激活剂mitapivat,用于治疗丙酮酸激酶(PK)缺乏症成人患者。它的新药申请已经获得FDA授予的优先审评资格。Reata Pharmaceuticals公司的口服核因子红细胞2相关因子(Nrf2)激动剂,用于治疗阿尔波特综合症(Alport Syndrome,AS)相关的慢性肾病患者。吉利德科学公司的长效HIV-1衣壳抑制剂lenacapavir,用于治疗接受过多次治疗,并且对多种药物产生耐药性的HIV-1感染者。吉利德指出,如果获批,lenacapavir将成为首款获批的衣壳抑制剂,也将成为首款每隔6个月给药的HIV-1治疗选择。Marinus Pharmaceuticals公司的GABAA受体阳性别构调节剂ganaxolone,用于治疗与CDKL5缺乏症(CDD)相关癫痫发作。它已经获得FDA授予的优先审评资格。默沙东(MSD)公司的口服选择性P2X3受体拮抗剂gefapixant(MK-7264),用于治疗慢性咳嗽。Akebia Therapeutics与田边三菱制药株式会社(Mitsubishi Tanabe Pharma Corporation)联合开发的口服低氧诱导因子脯氨酰羟化酶抑制剂vadadustat,用于治疗肾性贫血。这些创新疗法的临床试验和监管审评能否顺利进行,为患者带来更多更好的治疗选择?新的一年里让我们一起见证。
参考资料:
[1] The biotech scorecard for the first quarter: 19 stock-moving events to watch. Retrieved January 3, 2022, from https://www.statnews.com/2022/01/03/the-biotech-scorecard-for-the-first-quarter-19-stock-moving-events-to-watch/
[2] 各公司官网
文章来源:药明康德








