

癌症正成为全球病患死亡的主要原因和公共卫生的主要问题。根据此前IARC所发布的《2020年全球最新癌症负担数据》显示,2020年全球癌症死亡病例约996万例,而其中,中国癌症死亡人数就高达300万,占比约30%,居全球首位。
如果能在癌症患者早期及时发现并给予干预和治疗,将会大幅提升患者存活率与治愈率。因此,癌症的早期筛查十分必要。目前癌症早筛中血液肿瘤生物标志物的手段较为常见,其灵敏度和特异性却始终差强人意。
近日,四川大学国家生物医学材料工程技术研究中心、复旦大学附属中山医院等多家单位在Nature Communications上联合发表了最新研究成果——《Multiplexed nanomaterial-assisted laser desorption/ionization for pan-cancer diagnosis and classification》(多重纳米材料辅助激光解吸电离在泛肿瘤诊断和分类中的应用)。
此研究介绍了一种基于纳米材料辅助的高通量质谱技术结合机器学习的新技术。该方法仅需微量血清,且前处理方式简单可重复,具有低成本、高通量、高准确率的优势,被认为其在癌症诊断等标准临床实践中拥有巨大潜力。这一研究成果极大可能会为癌症的诊断和筛查带来技术上的突破与进步,成为提高癌症检出率和提高生存时间的一大利器。
本文第一单位四川大学国家生物医学材料工程技术研究中心主任王云兵教授介绍到:“在这项研究中,我们开发了一种全新的泛癌症诊断方法,并称之为‘Multiplexed Nanomaterial-Assisted LDI for Cancer Identification (MNALCI,多重纳米材料辅助LDI癌症识别)’技术。在论文中,我们定制了两种特殊形貌、结构和性能的纳米材料并应用于高通量飞行时间质谱,使其可以捕获和分析小分子代谢物的信号,并有机结合人工智能机器学习算法,在六种最常见癌症(包括肺癌、肝癌、甲状腺癌、肠癌、胃癌和胰腺癌)的诊断和分类上都有着非常巨大的潜力。”
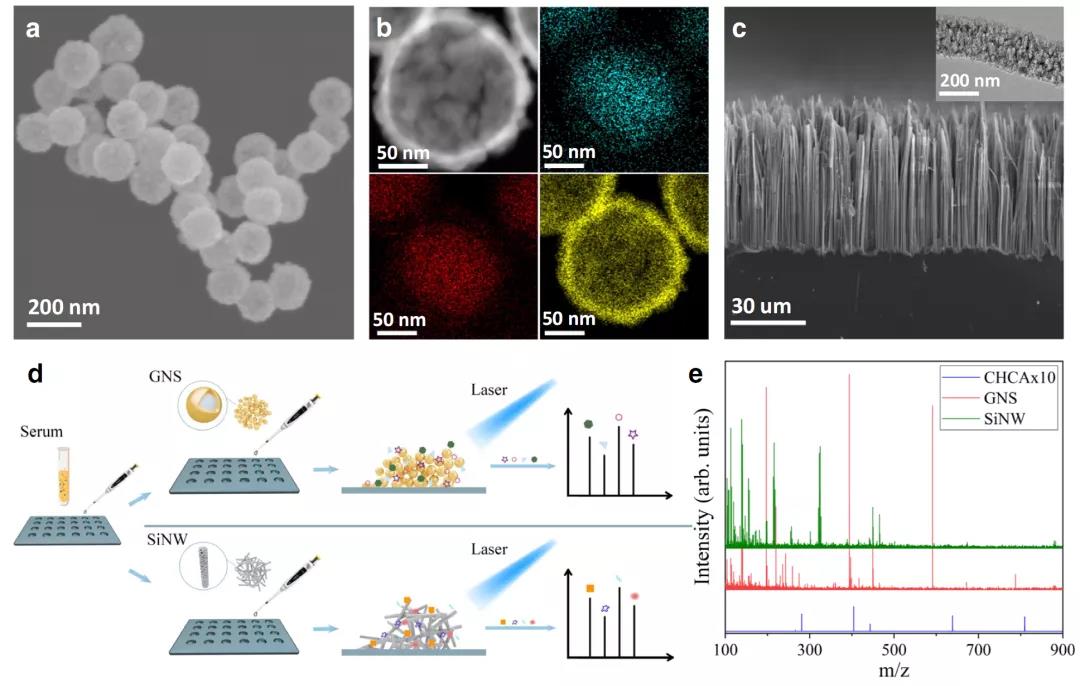
图1 | 两种纳米材料的表征与性能
该研究使用了两种纳米材料进行LDI-MS检测,以生成血清样品中代谢物的特征指纹图谱。第一种纳米材料是SiO2-Au核壳结构。金纳米壳层(GNS)在LDI中的应用性能优于其它金纳米结构,这与金纳米壳层粗糙的表面和强的表面等离子体效应有关;第二种纳米材料是由n型硅晶片经Ag辅助的化学腐蚀制备而成的高密度的多孔硅纳米线(SiNW)。多孔硅纳米线以前用于LDI-MS的小分子分析,使疏水表面具有更高的LDI效率。
MNALCI技术在两种纳米材料辅助LDI的基础上建立起来,并在以复旦大学附属中山医院为牵头的中国两家医院的大样本人群中进行了结合临床的研究。
根据美国癌症联合委员会癌症分期标准,此研究纳入了805例病理证实为恶性肿瘤的患者,以及203例的健康对照,同时建立了外部验证集群——纳入该研究的六种癌症均属中国十大常见癌症。
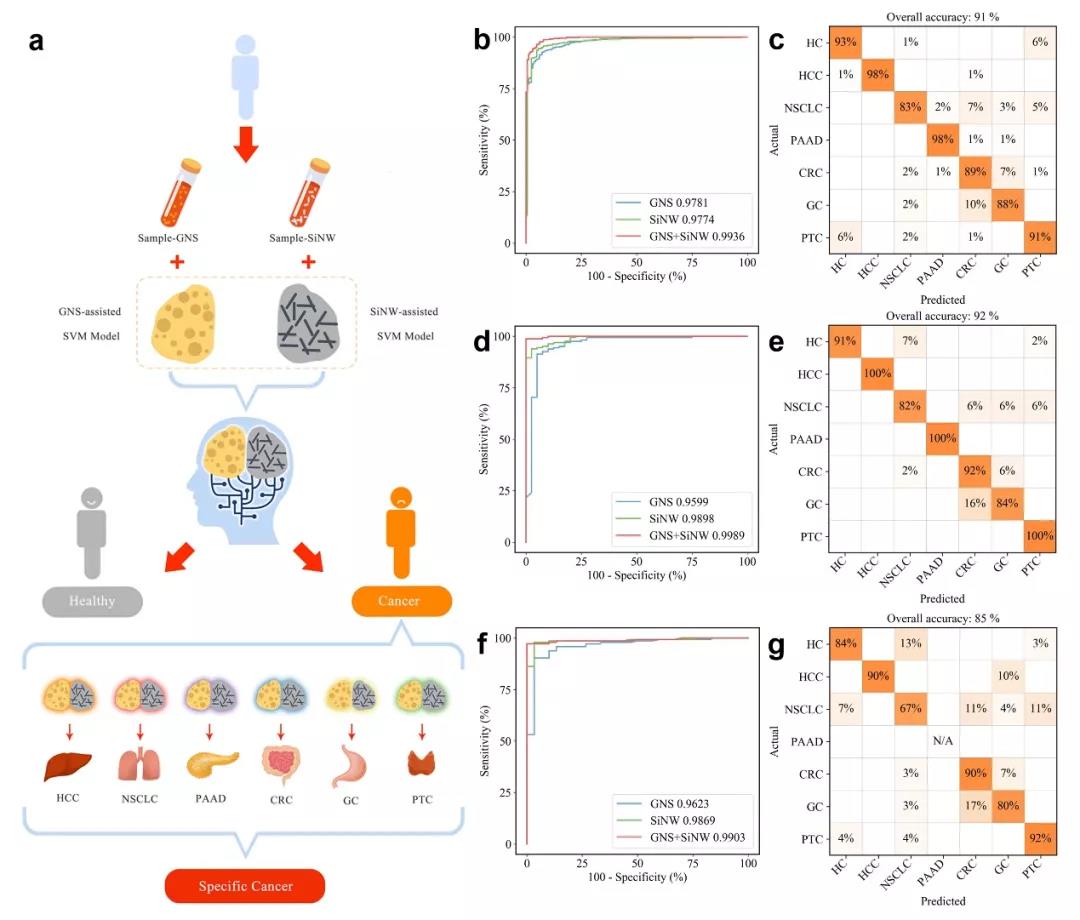
图2 | MNALCI方法及其准确率
在血清样本中,两种不同的纳米结构结合飞行时间质谱检测都产生了千级以上的信号峰,这其中的许多信号在癌症组和对照组中仅有细微的变化,这就需要结合人工智能算法进行筛选和区分。该研究采用SVM递归特征消除法,将变量按权重进行排序,并设计了两步SVM程序来建立 “代谢指纹图谱”。
该算法首先将癌症患者样本与健康对照组区分,结合GNS和SiNW的融合模型在受试者工作特征(ROC)曲线的曲线下面积(AUC)为0.994,优于单独使用GNS或SiNW辅助模型。在区分了癌症患者和健康对照者之后,使用第二个SVM分类器对六种不同的癌症进一步分类。从混和矩阵中可以看出,在93%的特异性下,融合模型在各种癌症分类中的整体准确率为91%,在不同的癌症类型和对照组中,以肝细胞肝癌和胰腺导管癌的准确率为最高的98%,而非小细胞肺腺癌的个体准确率为最低的83%。
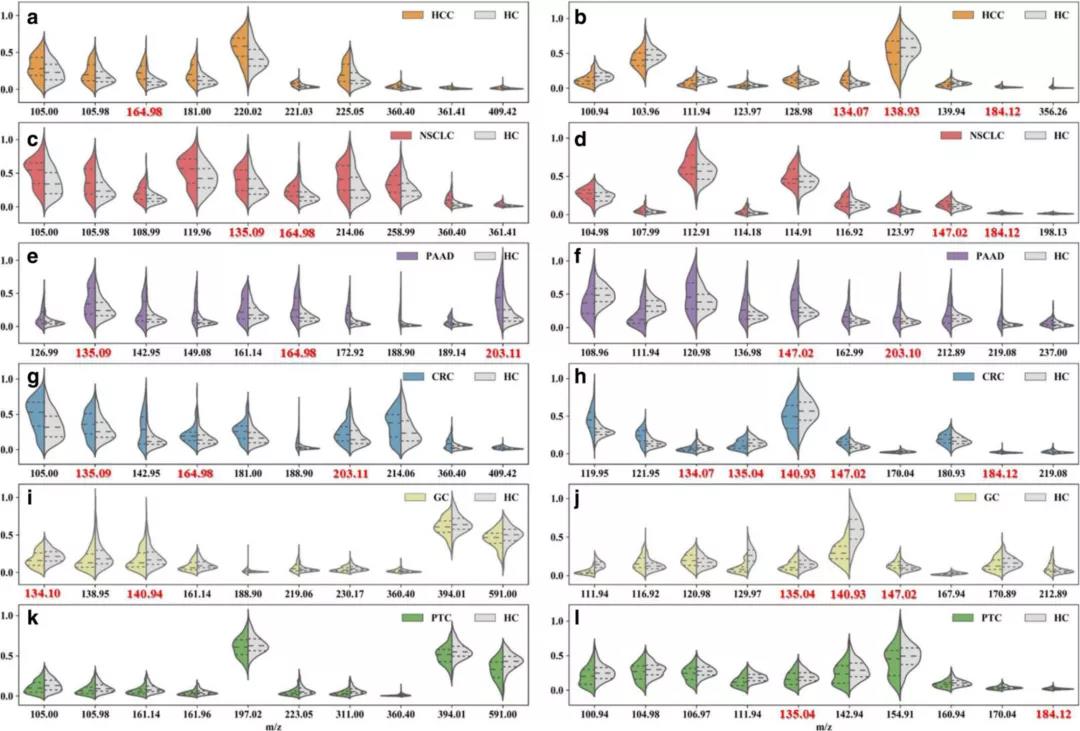
图3 | 癌症和健康对照的指纹图谱差异
除了癌症的诊断和分类,MNALCI还为筛选潜在的小分子生物标志物提供了重要的线索。通过对癌症患者和健康对照组的训练之后,该研究进一步分别选取了区分每种癌症类型及其对照组的前10大权重的“物质”及其对应的P值;还在此基础上得出了具有前30个特征的热点图,可以直观地看到6种癌症类型之间的差异以及与健康对照组间的差异。通过不同的m/z值集合表征的独特代谢产物筛选出了每种癌症患者的血液循环中发现的代谢产物差异。
癌症的早期诊断迫切需要非侵入性筛查解决方案,由于代谢改变可直接参与转化过程或支持使肿瘤生长的生物学过程,小分子代谢物可成为癌症特异性信息的独特来源。代谢组学临床肿瘤研究应用已经成为一个迅速增长的领域。目前癌症代谢组学在很大程度上运用于靶向性研究,可以被检测和识别的分子是有限的。相比之下,非靶向的LDI质谱技术则具有及时分析、高通量、低样本消耗等特点,是一种非常有前途的无创癌症诊断解决方案。同时,定制化纳米材料与高通量质谱技术及人工智能机器学习算法相结合,使其可以捕获和分析小分子代谢物的信号,在多种癌症诊断和分类上都有着非常巨大的潜力。
MNALCI这一独特的方法针对不同类型的癌症,建立了一个仅需微量血清,成本更低、周期更短、通量更高的检测方式,同时具备高灵敏度和高特异性的优势,为癌症的临床诊断提供了新的方向和可能。该MNALCI技术采用非靶向半定量质谱衍生的生化特征进行诊断,MNALCI不是依赖于单一的生物标志物,在理论上可以利用其检测到的所有信号。
该方法可以与基于其他生物标志物的筛选策略相结合,多种液体活检策略的结合可以提供额外的信息,进一步提高其诊断癌症和识别肿瘤组织来源的准确性。该研究为低成本高效率以及高通量的泛癌筛查技术奠定了理论和实践基础。早期发现这些癌症可以降低总体死亡率,从而大大减轻公共卫生负担。随着泛癌症早筛技术的不断突破,癌症对于人类的致死威胁也在不断降低,未来人们将不再“谈癌色变”!
文章来源:动脉橙果局

