以下文章来源于:医药投资部落
2022年12月28日,云顶新耀宣布,其位于浙江嘉善的全球生产基地一期项目暨mRNA疫苗产业化基地正式投入运行,并且进行了成功的试生产。该mRNA疫苗产业化基地占地面积85亩,建筑面积达58,000平方米,投资规模超过9亿人民币,拥有全套的先进生产设施和完善质量保障体系,达产后,年产能预计可达7亿剂次mRNA疫苗产品,将为云顶新耀实现mRNA技术平台的本土化研发、生产以及商业化运营奠定坚实的基础。此前的12月15日,云顶新耀宣布,公司自主研发的mRNA狂犬病疫苗项目,在免疫原性等临床前研究中取得了积极结果,已达到其临床前概念验证的里程碑。这两件mRNA技术平台的里程碑式的事件,也标志着,自从2021年9月与Providence达成关于mRNA技术平台的全面战略合作,在短短一年多的时间内,云顶新耀用远超业界预期的速度,完成了集研发、临床、生产于一体的对mRNA技术平台全产业链布局,成为国内稀缺的拥有自主可控的mRNA技术全平台能力的企业之一。对于先进技术平台的成体系的全面引进与消化吸收,并且内化为企业自身的核心研发能力,而不是简单地引进一两款成熟的管线,这种显著的变化,昭示着云顶新耀在企业核心战略层面的全面转型与跃迁。这种全面的战略转型,或许从22年下半年的一系列的管线变化和人事调整上都显出些许的端倪。2022年9月19日,云顶新耀发布公告称,罗永庆先生已获委任为公司执行董事兼首席执行官,自当日起生效。公开资料显示,罗永庆先生在医药健康行业有超过二十五年的经验,从业经历极为丰富,其此前供职的药企,既包括默沙东、诺华、罗氏这样的跨国巨头药企,也包括吉利德、腾盛博药这样的Biotech类型企业,无论是哪种类型的企业,罗永庆先生都在其中取得了让行业为之侧目的优异业绩,属于“全能型CEO”。

图片1:云顶新耀新任CEO罗永庆先生
有业内人士这样评价罗永庆先生:兼具严谨的科学家素养与锐意进取的创业者精神,这种特质,也与云顶新耀当下兼顾守业与创业的企业战略需求不谋而合。新任CEO的到来,也给云顶新耀这家成立5年多的Biotech公司带来了全新的战略转型,云顶新耀正全面迈入自身的转折之年。综合罗永庆先生上任前后,云顶新耀各条业务线的大刀阔斧的调整与实质性的研发进展,我们可以发现,云顶新耀正从过往追求确定性的BD模式为主的战略,坚定地转向“BD与自研双轮驱动”的全新战略,对确定性和前瞻性的有效平衡与兼顾,正成为云顶新耀企业战略的核心。从这个最基本的企业战略出发,既可以更好地理解云顶新耀一系列业务调整背后的核心逻辑,也可以对其未来的发展路径有更清晰的认知与展望。2022年8月,云顶新耀发布公告,宣布与吉利德全资子公司Immunomedics签订协议,将公司此前从Immunomedics公司引进的重点管线Trop-2 ADC药物戈沙妥珠单抗在大中华区、韩国及部分东南亚国家的开发和商业化独家权利转回给Immunomedics,交易总金额高达4.55亿美元。这笔交易一度在二级市场引发轩然大波,很多对公司缺乏足够了解的投资者,认为云顶新耀“卖掉了未来”,由此也导致公司的股价出现了较大幅度的波动。然而,如果从“确定性与前瞻性”的战略角度来解读这笔交易,就会发现事实并非如此,甚至可以得出完全不一样的结论。2019年2月,云顶新耀从Immunomedics引进戈沙妥珠单抗,从之后这款ADC药物的极为成功的研发进展来看,毫无疑问这是一笔非常成功的交易。但是也应该看到,在2022年的中国市场,乳腺癌治疗领域的ADC药物的竞争激烈程度,正在以肉眼可见的速度加剧:不仅多款针对乳腺癌治疗的国产ADC药物正在陆续上市的过程中,一代“神药”DS8201也已经启动了进入中国市场的流程。在这种竞争格局下,再将核心资源投入到戈沙妥珠单抗的商业化,很难说还是一个明智的选择。但是将戈沙妥珠单抗卖回给Immunomedics,云顶新耀不仅将获得总额4.55亿美元的对价(预付款2.8亿美元和未来潜在的里程碑付款1.75亿),而且将无需再支付剩余里程碑付款7.1亿美元。从确定性的角度来说,这毫无疑问是一笔非常漂亮的交易:最大程度地规避了未来商业化的不确定性,同时最大程度地拥抱了现金流的确定性。这笔充满深度战略思考的交易,可以认为是云顶新耀发展过程中的重要转折点之一,即使放在整个中国医药产业的历史中来看,也是充满传奇色彩的一笔BD交易。但是如果对云顶新耀“兼顾确定性与前瞻性”这一基本战略没有深入的了解,可能就无法看懂这笔BD交易背后深刻的逻辑。事实上,云顶新耀更多的资源分配与管线发展战略,也是基于这一基本的战略出发点作出。在成立之后的5年多以来,云顶新耀以一系列让人眼花缭乱的成功BD交易,构筑了在同等规模的Biotech企业中堪称“豪华”的管线组合,不仅涉及多条技术路线,更是覆盖多种疾病治疗领域。但是云顶新耀绝对没有因此而失去战略焦点,相反,云顶新耀极其明确地提出了“聚焦肾病治疗和mRNA平台”的资源分配战略,其中,肾病治疗是公司拥有高度确定性优势的领域,mRNA平台则是公司前瞻性战略的集中体现。以IgA肾病为代表的肾小球疾病领域,是云顶新耀未来一段时间的资源聚焦的研发方向,这一战略方向的确立,一方面是云顶新耀对“巨大未被满足临床需求”的深刻洞察,另一方面则是基于云顶新耀既有的确定性管线优势。IgA肾病是一种自身免疫介导的慢性、进行性肾损伤疾病,是导致慢性肾脏病(CKD)和肾功能衰竭的主要病因。IgA肾病的发生呈现明显的地域性特征:在以中国为主的东亚地区高发,而在创新药发达的欧美地区则相对发生率较低。在中国乃至整个东亚地区市场,IgA肾病都是一个典型的的存在“巨大未被满足的临床需求”的细分市场。云顶新耀肾病产品组合中的主打候选产品Nefecon,是全球50年来首款针对IgA肾病的靶向治疗药物,也是一款在IgA肾病治疗领域具备划时代潜力的重磅药物。Nefecon是口服布地奈德迟释胶囊,这种新剂型可将布地奈德特异性递送至回肠的派尔集合淋巴结(负责产生分泌性免疫球蛋白A)处,从而抑制诱发IgA肾病的半乳糖缺陷的 IgA1抗体(Gd-IgA1)的产生,进而在发病机制上游阶段进行干预,治疗IgA肾病。2022年10月,Nefecon的关键性全球3期临床研究NefIgArd的A部分结果在《Kidney International》杂志全文发表。结果显示:在维持稳定RAS阻断剂治疗的基础上,治疗9个月后,Nefecon组的尿蛋白肌酐比(UPCR)与安慰剂组相比降低了27% (P = 0.0003) ,Nefecon组和安慰剂组的UPCR较基线值分别减少31%和5%。在肾功能保护方面,治疗9个月后, Nefecon组的eGFR治疗获益达到3.87 ml/min/1.73 m2,具有统计学意义(P = 0.0014)。而在A部分研究数据截至时间点,部分患者完成了第12个月的随访,停药三个月后,患者的蛋白尿水平持续降低,较基线下降幅度达52%,患者持续受益。在今年4月份,云顶新耀公布中国人群亚组在接受Nefecon治疗9个月后,蛋白尿下降和稳定肾小球滤过率(eGFR)的结果,与关键性全球3期临床研究NefIgArd A部分的主要结果一致。2022年11月,云顶新耀向中国国家药品监督管理局提交Nefecon的新药上市许可申请(NDA),用于治疗具有进展风险的原发性IgA肾病(IgAN)成人患者,这标志着Nefecon距离成功在中国上市又前进了一大步。12月,国家药监局药品审评中心(CDE)在官网公示拟将其新药上市许可申请纳入优先审评,这将进一步加速审批进程。值得一提的是,Nefecon此前已在美国和欧盟获批上市,美国和欧盟的先期批准,以及循证医学证据的高度一致性,都为这款药物在中国的成功获批最大程度地增加了确定性。仅仅在中国大陆地区,就有约400万~500万的IgA肾病患者,而云顶新耀拥有Nefecon在大中华区、新加坡和韩国的独家商业化权利。一旦Nefecon成功在中国获批上市,面对完全蓝海的IgA肾病领域,这款药物相当于创造了一个全新的市场,其潜在的商业化的高度非常值得市场期待。除了Nefecon以外,云顶新耀的肾病创新治疗管线组合中,还有多个潜在的重磅品种。2022年9月,云顶新耀的另一款候选产品EVER001获得了中国国家药品监督管理局对其1b期临床试验(IND)申请的批准。EVER001是新一代共价可逆的布鲁顿酪氨酸激酶(BTK)抑制剂,正在开发用于治疗以蛋白尿为特征的肾小球疾病。此外,云顶新耀还有多个肾病研发项目正处于临床前阶段,其中进展最快的一款针对肾小球肾病的候选药物,预计将在未来两年内提交临床试验申请。从云顶新耀肾病治疗管线的组成来看,也充分体现了“兼顾确定性与前瞻性”的特征:即将商业化的Nefecon作为确定性非常强的管线,是云顶新耀当前肾病治疗业务线的基石产品,而更多在研产品作为前瞻性的布局,为肾病治疗业务更长远的发展打下基础。如果说肾病治疗管线的布局,体现了云顶新耀对于确定性的不懈追求,mRNA平台则充分体现了云顶新耀的前瞻性战略。毫不夸张地说,mRNA技术是近年来全球制药工业革命性的突破方向之一,而新冠疫情又将mRNA技术的巨大的商业化可能性加速呈现在整个行业面前,在行业领先者们获得巨大的收益后,已经无人再怀疑mRNA技术广阔的前景。云顶新耀的mRNA技术,引进自合作伙伴Providence;虽然Providence只是一家小型的Biotech公司,但是其核心成员拥有在全球mRNA技术领域十多年的研发经验和技术积累,其mRNA技术平台完全不逊色于大家耳熟能详的几家国外mRNA巨头。目前,云顶新耀的mRNA相关管线中,进展最快的是新冠疫苗PTX-COVID19-B。2022年10月19日,云顶新耀宣布,旗下mRNA新冠候选疫苗PTX-COVID19-B在评估其安全性、耐受性和免疫原性的II期研究中取得积极的顶线结果。数据显示,PTX-COVID19-B在第二剂肌内注射接种两周后观察到的中和抗体几何平均滴度(GMT)比值方面,与美国FDA批准的mRNA疫苗Comirnaty®(由辉瑞和BioNTech共同研发)达到统计学非劣效。云顶新耀对外表示,这是第一项直接将候选mRNA疫苗与已获批mRNA疫苗进行头对头对比的临床研究,其结果让人振奋,在PTX-COVID19-B这款初级免疫疫苗的基础上,云顶新耀开发了另一款针对奥密克戎(Omicron)的二价加强针候选疫苗EVER-COVID19-M1.2,计划于2023年在中国启动临床试验并拟于年底前申请紧急使用授权(EUA)。值得注意的是,云顶新耀并非简单地从合作伙伴Providence引进一两款mRNA技术路径的管线,而是成体系地引进了全套的mRNA技术平台,并在最短的时间内组织技术团队攻关,吃透相关核心技术环节,并内化为自身的核心能力。
图片2:云顶新耀mRNA生产车间一角
目前,随着嘉善生产基地的全面投入运营,云顶新耀已经拥有了从最初的抗原设计直到后端规模化生产的mRNA技术全产业链能力,成为国内稀缺的拥有自主可控的mRNA平台技术能力的Biotech企业。除了在管线的资源分配上可以明显感受到云顶新耀在确定性与前瞻性之间力求平衡,在BD和自研这两种模式的抉择上,我们亦可以发现云顶新耀兼顾确定性与前瞻性的决心。云顶新耀在BD领域的巨大优势已不必赘述,公司在过往5年以来多项成功的BD交易记录,是其卓越的BD能力的最好证据。但是也必须承认,BD引进成熟管线的模式,在提供了确定性的同时,相比于原研模式,确实在前瞻性或者说想象空间上稍逊一筹。事实上,云顶新耀自成立伊始,就确定了要做自研的战略,并且为此进行了长期的资源储备,目前也终于到了将自研战略全面提上日程的时点。2022年2月18日,云顶新耀的新药研发中心在张江科学城落成并投入使用,作为云顶新耀战略布局的首个新药研发中心,该中心将充分利用上海生物医药发展的区位优势,开启并加速云顶新耀创新药自主研发的进程。

图片3:云顶新耀位于张江科学城的新药研发中心
据介绍,云顶新耀的药物发现和转化医学团队逐渐搭建成形,团队汇聚了行业内新药研发的顶尖科研人才,其中半数以上拥有博士学位及海外留学工作经历。研发团队已经入驻新药研发中心,聚焦肾病、mRNA疫苗领域的新药研发,致力于研发和创建全球“同类首创”或“同类最佳”的创新药管线。此外,化学制造与控制(CMC)团队也已经入驻新启用的研发中心,这标志着云顶新耀已经组建了从前期化合物筛选到后期生产制造的全环节的自研团队。目前,自研业务线诸多管线的里程碑式进展,也标志着云顶新耀已经从过往的以BD引进管线为主,彻底转变为“BD引进+自主研发”的双轮驱动模式。当然,无论是BD引进,还是自主研发,都是满足未被满足临床需求的具体实现手段,二者不存在孰优孰劣的问题,云顶新耀的这一战略转型,其背后本质的思考还是确定性与前瞻性的平衡问题。对于未被满足的临床需求,如果能够以合适的对价引进合作伙伴的成熟管线或技术平台,这种经过科学评估之后的确定性,仍然将是一段时间内云顶新耀追求的目标;但如果对于某些特定的临床需求,全球范围内都不存在可引进的成熟管线,而云顶新耀的技术平台和自研团队又具备相关领域的特定优势,那么云顶新耀也将遵循科学规范的立项流程,坚决投入资源进行前瞻性的布局和自主研发。一切决策的依据,都是如何以更高效务实的方式,满足未被满足的临床需求,在云顶新耀的决策体系中,这是最为根本的出发点。中国创新药产业发展至今,已经从最初的躁动与兴奋中逐渐回归行业的本质:如何更好地满足未被满足的临床需求。云顶新耀正是基于这一根本的出发点,在新任CEO的带领下,大踏步迈入自身的战略转折之年:以快速商业化的管线打造企业的确定性,以基于临床需求洞察的自研管线构筑企业的前瞻性。这种战略在稳健与进取之间求得可贵的平衡,既不落于保守也不失之冒进,这不仅是基于云顶新耀自身资源禀赋的合理战略安排,也契合了当下中国创新药产业发展的内在要求。
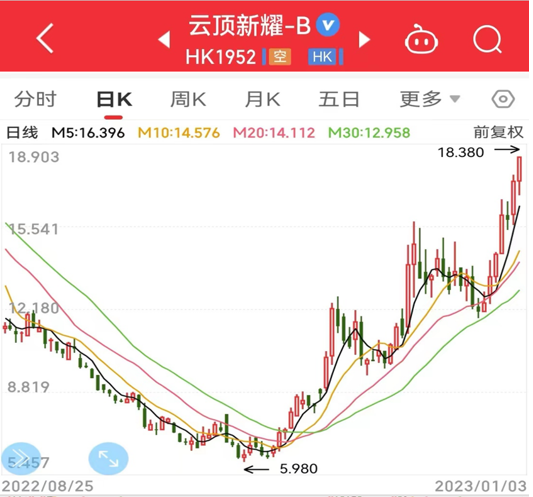
云顶新耀这种兼顾确定性与前瞻性的全新战略,其价值也正在被市场逐步的认知:在新任CEO罗永庆先生上任之后的三个多月以来,公司股价强势反弹,目前股价相对最低点上涨幅度超过200%,是近期港股Biotech板块反弹趋势最为迅猛的领涨股之一。不过,仅仅55亿港币的市值,也许只是云顶新耀价值回归之途的开始。在成立之后的第一个5年,云顶新耀已经交出一份靓丽的答卷,我们有理由相信,在全新开局的第二个5年,云顶新耀巨大的潜力将会给中国医药产业带来更多的惊喜。







