在宣布管线合作整整2年之后,恒瑞医药和昔日合作伙伴万春医药走到了诉讼阶段。
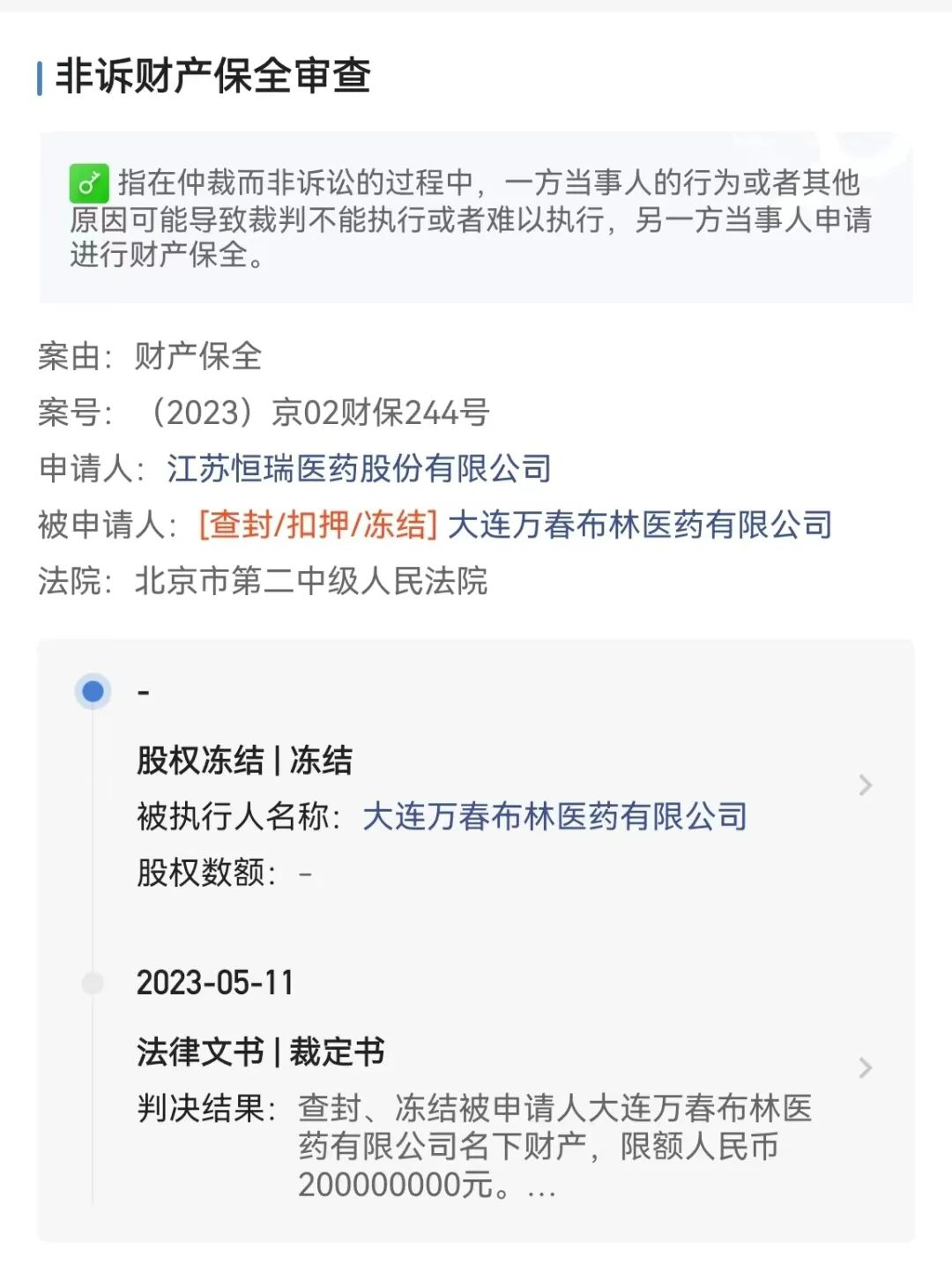
近日,一则恒瑞医药要求法院冻结万春医药2亿元的财产保全公告,再次将恒瑞医药和万春医药之间的陈年旧案推到台前。
2021年8月25日,刚刚开启BD战略的A股"医药一哥"恒瑞医药,与万春医药子公司大连万春签订战略合作协议。根据协议,恒瑞医药将对大连万春进行1亿人民币股权投资,并支付总计不超过13亿人民币的首付款和里程碑款,以获得大连万春GEF-H1激活剂普那布林在大中华地区的联合开发权益以及独家商业化权益。普那布林是万春医药开发的1类创新药,属于GEF-H1(鸟嘌呤核苷酸交换因子)激活剂,能促进骨髓细胞成熟,防止化疗对中性粒细胞的损伤,以达到早期控制CIN的疗效。普那布林属于非G-CSF类药物,与G-CSF具有机制互补性,全球多中心临床试验证明,普那布林联用长效G-CSF可显著降低重度CIN的发生率。正好,恒瑞医药已有一款长效G-CSF创新药硫培非格司亭(商品名:艾多)获批上市,如果能将两者的优势结合起来,极有可能产生"1+1>2"的临床价值。消息传出,万春医药股价最高冲到33美元/股,市值超过10亿美元。
当时极少有人意识到,此刻已是这家2017年就登陆纳斯达克的中国药企,在美股最后的余晖。仅仅在3个多月以后,被市场普遍认为有望成为30年以来CIN领域重磅突破性治疗品种的普那布林,被FDA拒绝在美国上市。FDA拒绝的理由,是认为现有三期注册临床不能充分证明治疗获益,要求万春医药进行第二项注册临床,以获得充分证据支持CIN适应症的获批。有市场分析人士认为,普那布林的III期临床入组患者中,13%来自美国和澳大利亚,87%来自中国,在FDA无比强调"临床入组多样性"的当下,主要来源于中国患者的临床数据去冲关FDA,本来就凶多吉少。同时,入组患者中仅有15%接受了一线疗法的PD-1治疗,而2、3线NSCLC患者指的是在接受一线治疗失败后再使用二线三线治疗方法的患者。因此,普那布林入组患者既体现多元化,也不能代表当前标准下的二三线NSCLC患者,被FDA拒绝,也在情理之中。普那布林美国上市遇挫,也给刚刚启动对外BD战略的恒瑞医药带来了不大不小的尴尬。
2021年12月2日,恒瑞在公告中回应称,根据双方签署的《普那布林产品合作协议》,恒瑞医药已向万春布林支付了2亿元人民币首付款,关于《增资入股协议》所约定的拟向大连万春进行的1亿元人民币股权投资,恒瑞尚未缴款,股权也未交割。从双方公布的合作信息来看,此次恒瑞医药要求保全的这2亿元,应该是当初支付给万春医药的首付款。根据万春医药在美股公开的财务报表信息,截至2022年底,其账上现金以及现金等价物约2.46亿人民币。
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。

