国内有没有生物医药基础研究?
这只能露出尴尬而不失礼貌的微笑。国内没有类似NIH的机构,基础研究主要由公立大学及学术机构承担。你在北大医学部科研网页看见的都是得奖、发论文、申报项目及科研经费,还有抖音热播个别教授到处呼吁实行免费医疗。
其实,创新药的繁荣并非本土生物科技自然孕育的结果,而是海归科学家站在海外巨人的肩上推动的结果,新靶点、新机制、新技术、新药物形式主要来自于美国。
2021年,我国政府在所有自然科学领域基础研究的投入为1679亿元人民币,仅相当于美国NIH在2022年对生物医学领域基础研究的投入(据《中国科学院院刊》)。
NIH 2023财年预算增至490亿美元。
在基础研究无法提供原创靶点的现状下,国内创新药企不得不卷向海外存量靶点。
在跨国药企纷纷折戟的难成药靶点上,比如SHP2、CD47、CD73、TIGIT、Trop-2(NSCLC适应症),国产创新药企寻觅“裂缝里的光”,分别通过单药、联合疗法、双抗或者ADC的形式重点布局,如果能够突破,将是创新药行业的划时代进步。
于是,我们看见满手死亡管线的Biotech。
01
基础研究,高校何为
NIH(国立卫生研究院)是美国基础研究投入的重要机构。
美国生物医药产业的繁荣来源于基础研究。2010年至2016年FDA批准的210个新药中,每一个成果(新药)都可以将原创性初始研究资源归结到由NIH资助的工作(据《美国国家科学院院报》)。
在获得首批新化合物(NMEs),特别是使用有针对性的药物发现方法(包括重组生物制剂以及靶向机理)用于发现NMEs新药之前,需要进行大规模的公共部门投资和重要领域的基础研究。统计数据表明,政府部门(主要通过NIH) 对从2010年至2016年批准的每种全新药物的研究平均投入高达8.39亿美元。其中,89%的成本与药物的靶向或机理研究成本相关,11%的成本与首创(First-in-class)药物合成及优化相关,或与化合物或后续合成及优化相关。
NIH的预算在2023财年增加43亿美元,几乎所有新资金都将流向ARPA-H(高级健康研究计划局),其最初的重点是癌症、糖尿病和阿尔茨海默病。这也昭示着创新药高景气的方向。
市场力量可比政府更好地将政府资助的技术商业化。美国高校把产生的知识有效地转移到私营部门,教授与工业界紧密合作,提高政府基础研究投入的转化效率。自1980年拜杜法案颁布以来,学术技术转让活动已为11000多家美国初创公司和200多种药物和疫苗的开发作出贡献。开发mRNA疫苗的关键技术即来自于宾夕法尼亚大学。
FIC或BIC管线有几个来自国内高校的原创?绿叶制药LY03005(若欣林)由烟台大学药学院转化,是中国首个自主研发的用于治疗抑郁症的化药1类创新药,作为一种 5-羟色胺(5-HT)、去甲肾上腺素(NE)和多巴胺 (DA) 三重再摄取抑制剂,仍然沿袭旧机制。60年来首款抑郁症新机制口服疗法——Auvelity(右美沙芬+安非他酮)缓释片去年8月获得FDA批准,研发企业Axsome当日股价上涨40%,至今没有跌回去。

02
死亡海域,博得够大
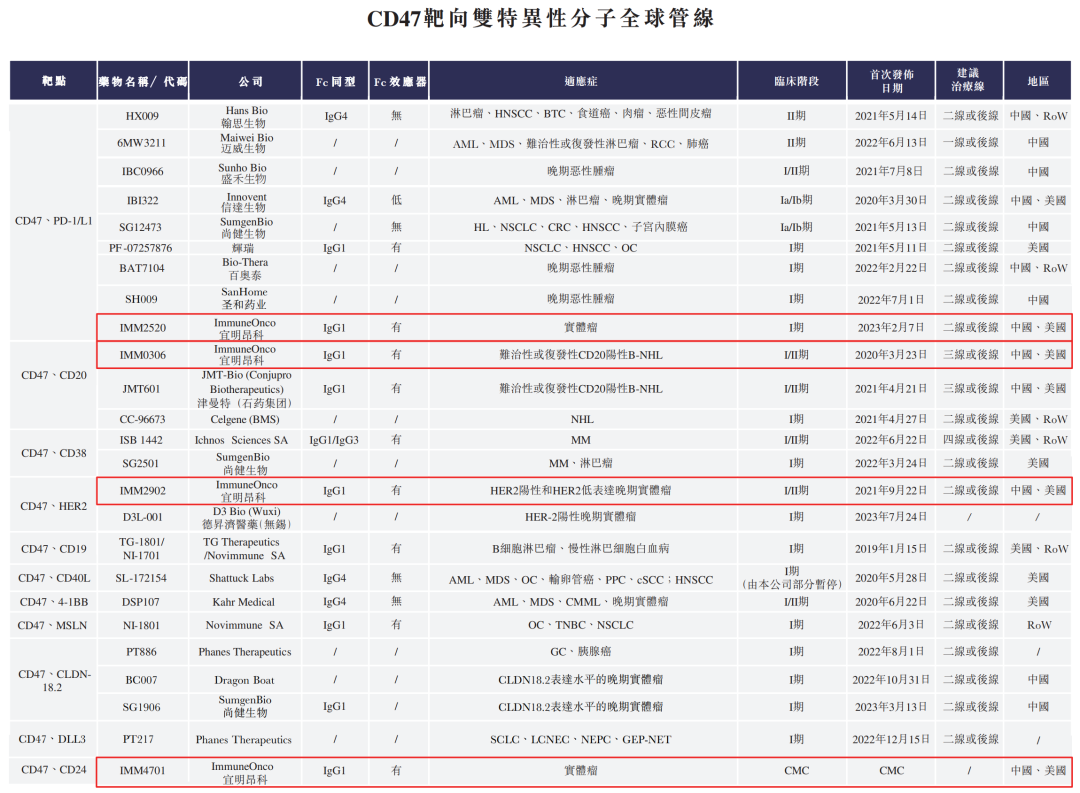
经过前面烘托,请出今天的主角。宜明昂科9月5日在港交所上市,All in CD47,被投资者称为“博得够大”。
CD47靶点至今仍是死亡海域,罗氏、艾伯维、吉利德、BMS(新基)纷纷遇挫。安全性一直是CD47抗体的首要问题,其与人体红细胞和血小板(普遍表达CD47)会有不可避免的结合,进而可能导致严重的血液毒性,如贫血、血小板减少症和血凝反应。许多临床阶段的CD47抗体已展现因与红细胞的结合活性,而导致严重的不良反应。
为解决安全性问题,几乎所有CD47抗体均使用与Fcγ受体结合能力较弱的Fc同型,如IgG4和IgG2。尽管这样的设计可能减少诱导巨噬细胞吞噬健康血细胞的风险,但使其对肿瘤细胞的免疫反应减弱,因此在CD47抗体临床试验中均未出现单药完全缓解(CR)。
CD47 靶点最近接近成药性的一次也失败了。吉利德莫洛利单抗联合阿扎胞苷联合治疗 MDS ,安全性数据良好,中期分析却发现有效性不足,全剧终。
CD47低毒性与有效性暂不可兼得。
被错付的明星靶点,据Insight数据库,目前国内有36 款CD47产品进入临床阶段,布局企业超过 30 家,其中,宜明昂科可能是赌性最大的Biotech,9条管线资产涉及CD47,如果靶点成药风险爆雷,不会有第二次犯错的机会。
不过,在国内基础研究薄弱的背景下,宜明昂科的管线布局仍然是正常的,属于中性事件。
1、既然无力开发原创靶点,那么只有对海外存量靶点进行改良,挑战MNC难成药的靶点,总比扎堆同质化好,也是差异化的一条路子。通过联合疗法、双抗或者ADC的改造,说不定有逆袭的可能。
2、综合型药企管线分散,可能拥有N次犯错的特权,但小型Biotech不适合大而全的平台型架构,聚焦于一个核心靶点,或者一种前沿技术,才是正常生态,当然爆雷归零也是正常生态。所以,宜明昂科专注于CD47并没有原罪。
这种逻辑传导到投资,意味着Biotech的风险教育还有待深入。投资创新药博的就是弹性,不是10倍的问题,而是0和10的问题。
宜明昂科在招股书中称其CD47核心产品IMM01“具有前景的单药有效性”,在I期单药治疗临床研究中的27例可评估患者中,确认了两例完全缓解(两例CR)、一例部分缓解(一例PR)及13例疾病稳定患者(包括六例观察到的肿瘤明显缩小病例)。在二期推荐剂量为2.0mg/kg的六例患者中,一例患者达到完全缓解(一例CR)及四例患者达到疾病稳定(四例SD)。其CR、ORR数据严重偏低。
IMM01单药已经没有前景。宜明昂科于2022年10月终止IMM01的II期单药治疗试验,把资源用于基于IMM01的联合疗法及基于CD47的双抗的临床开发。IMM01以2.0 mg/kg的剂量与阿扎胞苷联用三个治疗周期后的ORR达到93.8%。相比之下,天境生物的来佐利单抗、吉利德的莫洛利单抗及信达生物的IBI188各自以30 mg/kg的剂量水平与阿扎胞苷联用三个治疗周期后的ORR分别达到80.6%、90.9%及93.9%。
宜明昂科称,与全球管线中的其他CD47靶向分子相比,IMM01对CD47结合结构域进行特别改造,不会在体外与人体红细胞结合,并在I/II期临床试验中显示出对患者良好的安全性和耐受性。
事实上,海外大厂每一个遇挫的CD47分子在早期临床试验中几乎都有过美好时光。IMM01与阿扎胞苷联用将于2024Q1开始关键性临床试验,IMM0306(CD47×CD20)将于2024Q3开始关键性临床试验,0和10 的终极答案将揭晓。
康方生物CD47单抗AK117作为联合疗法核心管线,临床也在大规模推进。去年底《癌症免疫治疗杂志》发表的康方CD47单抗机制研究成果称,AK117无血凝作用,可诱导巨噬细胞对肿瘤细胞的强大吞噬作用,无需较低的预剂量来预防贫血,且抗肿瘤活性良好。
来源:阿基米德Biotech ,作者阿基米德君
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。

