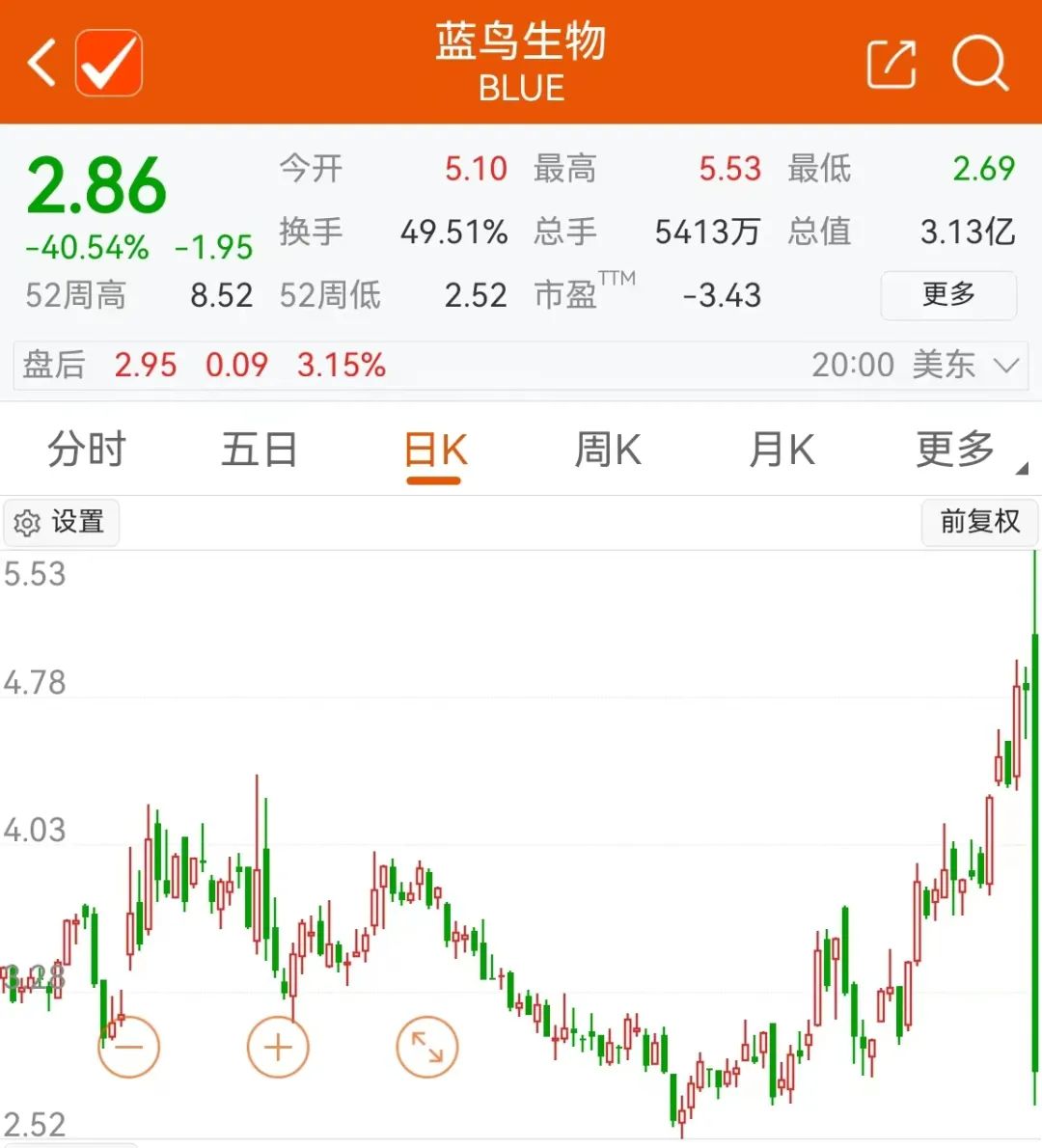
12月9日,在万众瞩目的首款CRISPR基因编辑疗法获批之际,作为背景板的老牌基因疗法研发企业蓝鸟生物的LYFGENIA疗法也获得了FDA的批准。但是消息传来,股价早已奄奄一息的蓝鸟生物,不仅没有迎来想象中的暴涨,反而直接下跌40%。
究其原因,在于同日获批的基于CRISPR/Cas9技术的基因疗法Casgevy,几乎直接宣告了蓝鸟生物的LYFGENIA疗法从此出局。首先,是二者的适应症完全一样:用于治疗 12 岁及以上患有复发性血管闭塞危象 (VOC) 的镰状细胞病 (SCD) 患者,属于头对头的竞争关系。根据公开信息,蓝鸟生物的LYFGENIA基因疗法目前定价为310万美元,而竞争对手的CASGEVY基因编辑疗法目前定价为220万美元。在此之前,蓝鸟生物基因疗法就因为昂贵的价格,面临商业化的巨大困难。2022年8月17日,蓝鸟生物(Bluebird bio)开发的用于治疗β-地中海贫血的基因疗法Zynteglo在美国上市,定价280万美元,成为全球最贵药物。仅仅一个月之后,蓝鸟生物第二款基因治疗药物Skysona获批上市,用于治疗4至17岁男孩罕见的神经系统疾病脑型肾上腺脑白质营养不良(CALD),定价300万美元。虽然不断刷新“全球最贵药物”的记录,但是这并未给蓝鸟生物带来任何实质获益,相反,由于过于昂贵的价格,蓝鸟生物已经基本退出了欧洲市场。
事实上,在获得FDA批准之前,2019年5月和2021年7月,Zynteglo和Skysona先后在欧盟获批上市,然而在2021年4月,Zynteglo2021从德国撤市,随后在2022年初更广泛地撤出欧洲市场;Skysona则上市不到三个月,就由于商业策略原因,或者说详细一些,由于谈判承保范围方面遇到困难而退出欧洲市场。也正是基于这样的商业化困境,蓝鸟生物的股价,从最高的152美元/股,飞流直下,暴跌到最低的2.52美元/股。2023年5月9日,蓝鸟生物公布2023年一季报,数据显示其在美国的商业化情况同样不容乐观:截至2023年3月31日,公司营收238.1万美元,同比增长22%;其中产品收入同比增长63%,达到230万美元。此次是蓝鸟生物的第三款基因疗法获得FDA批准上市,但是价格直接比竞争对手高90万美元,基本直接扼杀了其第三款基因疗法的商业化想象空间。
更为致命的是,此次蓝鸟生物获批的LYFGENIA疗法,还伴随着FDA的黑框警告:根据临床试验数据,该疗法有一定的致癌风险。作为基因疗法的先驱,蓝鸟生物自成立以来十余年,已经耗费了超过30亿美元的研发费用,虽然有三款基因疗法获得FDA批准上市,但是公司仍然面临着1年以内现金耗尽的窘境。蓝鸟生物面临的,是目前整个细胞与基因治疗赛道的共同困境:高昂的研发费用,高风险的临床试验,产品获批之后天价的费用和寥寥无几的病人,以及与之对应的居高不下的制备成本。虽然CGT赛道具备极大的科学价值,但是从商业化角度来说,其距离成熟阶段还有很大的距离。
2023年初,位于英国的全球制药巨头葛兰素史克(GSK)明确地宣布:终止在细胞与基因疗法方向的研发投入。
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。