近日,信达生物宣布其研发的IBI311,在中国开展的甲状腺眼病(TED)3期临床研究RESTORE-1达成主要终点,并计划向国家药监局提交新药上市申请。
值得一提的是,国内外多项临床治疗指南已将靶向IGF-1R抗体生物制剂列入推荐治疗方案,尤其对合并显著突眼的TED,靶向IGF-1R抗体生物制剂可作为首选,但国内尚无用于治疗TED的靶向药物获批。
新药上市在即,信达生物能否一举拿下总产品收入200亿元的目标?
01
打破孤品神话,
信达率先发起冲锋
资料显示,Teprotumumab是美国FDA批准的首个且唯一一个用于治疗甲状腺相关眼病的抗体药物,然而,在Teprotumumab获批上市之前,却拥有颠沛流离的命运。
肿瘤临床失败,免疫逆袭成王。2005年,Genmab开发出IGF-1R抗体药R1507(Teprotumumab),同年,罗氏获得该药开发权益并提交肿瘤适应症的临床试验申请。
然而,R1507用于治疗非小细胞肺癌(NSCLC)的2期临床试验显示,9mg/kg剂量组OS为35.1%,PFS为71.9%;16mg/kg剂量组OS为52.4%,PFS为63.2%,与安慰剂组(OS为35.1%,PFS为68.4%)对照均无显著改善。
此外,R1507对KRAS突变肿瘤同样无选择性差异,且在肉瘤的2期临床试验中,虽达到PFS终点,但作用有限,因此,罗氏放弃了肿瘤适应症的开发。
2012年,罗氏分拆旗下业务部门,River Vision获得该药开发权益并应用于眼科治疗(Teprotumumab),自此唤醒了其富贵“人生”,2017年,Horizon以1.45亿美元收购River Vision获得该药,2020年1月,Teprotumumab获美国FDA批准上市,商品名为TEPEZZA,成为治疗TED的全球孤品。
出道即巅峰,获MNC青睐。在2020年1月获批上市的TEPEZZA,用一个非完整年度的时间就达到了8.2亿美元的销售额,2022年销售额达19.66亿美元,增长139.76%,也让Horizon年度业绩以十亿美元量级持续增长,收入由2019年的13亿美元增长至2021年的32亿美元。
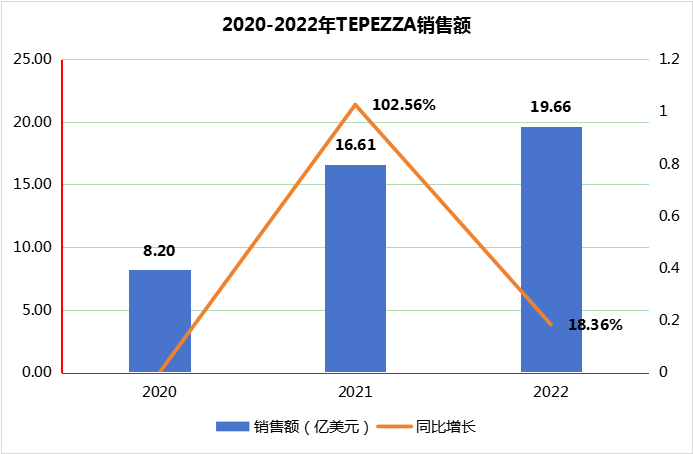
图1 2020-2022年TEPEZZA销售额
数据来源:Horizon财报
TEPEZZA在市场上惊人的表现,让MNC也为之心动,2023年10月,安进以约278亿美元的交易总价完成对Horizon的收购,将TEPEZZA纳入麾下,加强其在炎症药物领域的领先地位。据安进2023年Q4季报显示,第四季度,TEPEZZA得益于美国FDA批准的自我给药一次性预填充笔,销量较上一季度增长18%。
打破孤品神话,信达率先发起冲锋。目前全球仅有6款靶向IGF-1R的TED药物处于临床阶段,其中进展最快的为ImmunoGen/赛诺菲的AVE-1642,但仍处3期临床。
表1 靶向IGF-1R的TED药物临床进展
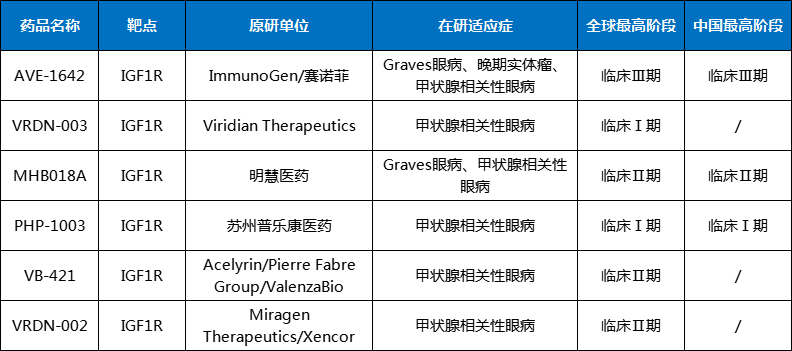
数据来源:药智数据
据IBI311临床数据显示,第24周时,主要研究终点眼球突出应答率治疗组和安慰剂组分别为85.8%和3.8%,关键次要研究终点眼球总体应答率,治疗组也显著优于安慰剂组,信达生物有了足够率先发起打破TEPEZZA全球孤品格局的实力。
02
实力雄厚,
专挑突破性产品下手
除计划提交NDA的IBI311外,2023年以来,信达生物已有6款新药获批或处于NDA阶段,其中,伊基奥仑赛和托莱西单抗获国家药监局批准上市,帕萨利司片、泰莱替尼、IBI-351和玛仕度肽NDA获国家药监局受理。
表2 2023年以来NDA获批/受理新药
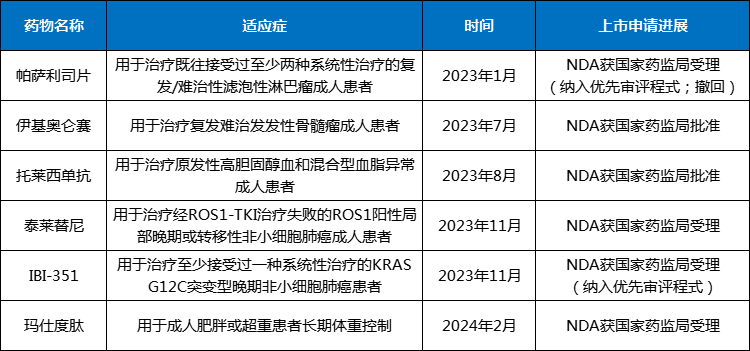
数据来源:根据信达生物公告整理
突破性治疗药物较多,竞争实力雄厚。上图6款药物中,多款药物将为国内患者带来变革性治疗手段。
伊基奥仑赛作为国内首款获批的BCMA CAR-T产品,具有强效持久疗效,据临床数据显示,客观缓解率(ORR)达96%,严格意义完全缓解/完全缓解率(sCR/CR)为74.3%,中位达缓解时间(mTTR)仅16天,12个月中位无进展生存期率(PFS)为78.8%;12例既往接受过CAR-T治疗患者中,9例获得CR,5例获得sCR,其中4例维持sCR超18个月。
泰莱替尼是新一代潜在最佳的ROS1 TKI,曾获国家药监局和美国FDA授予突破性疗法认定,据2期TRUST-II研究数据显示,在初治患者(n=25)中,经确认的客观缓解率(cORR)达92%;在既往接受过1种ROS1-TKI抑制剂治疗的患者(n=21)中,cORR为57%。此外,对存在脑转移患者(n=8)也有效,cORR为62.5%。
IBI351是中国首个NDA获受理的KRAS G12C抑制剂,单药在至少一线系统治疗失败携带KRAS G12C突变晚期肺癌2期临床试验中展示了优异的疗效,数据显示,客观缓解率(ORR)达46.6%,疾病控制率(DCR)达90.5%,中位缓解持续时间(DoR)为8.3个月,中位无进展生存期(PFS)为8.3个月。
此外,IBI351还被国家药监局纳入治疗KRAS G12C突变晚期结直肠癌的突破性治疗品种。
产品管线信心十足,延迟获批也不惧。按理说,新药越早获批上市,越能尽早商业化占据市场,信达生物的帕萨利司片用于治疗既往接受过至少两种系统性治疗的复发/难治性滤泡性淋巴瘤成人患者的上市申请,在2023年1月不仅获国家药监局受理,且被纳入优先审评程式,但在2023年9月,其主动撤回上市申请。
信达生物作出撤回决定是由于合作方对产品海外开发策略调整,基于整体研发策略和产品价值管理考量。据药智数据显示,帕萨利司片还有复发性/难治性非霍奇金淋巴瘤、骨髓纤维和边缘区淋巴瘤的临床管线试验已处于3期阶段。
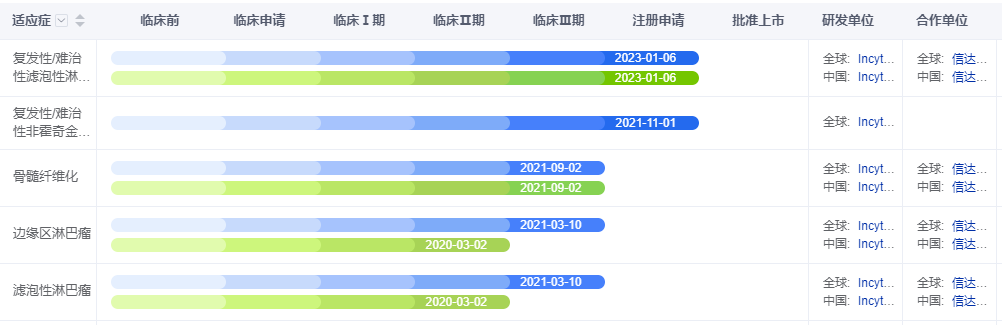
图2 帕萨利司片适应症3期临床试验进展情况
图片来源:药智数据
拥有较多突破性治疗产品的信达生物,未来几年也将再商业化出肿瘤癌症领域的重磅产品。
03
200亿产品收入的梦,
能否成真?
信达生物在2023年1月的JPM汇报中,提出了有望在未来5年实现产品收入200亿元的目标,据其2022年报显示,全年产品收入超41亿元,仅为目标金额的五分之一,要想梦想成真,复合增长率至少要保持在37%以上。
作为从Biotech向Biopharma转型的药企,信达生物也算是相当成功,截至目前,已有10款产品获批上市。
肿瘤业务虽强,还需向目标发起冲锋。信达生物的产品绝大多数为肿瘤癌症产品,其中,信迪利单抗、贝伐珠单抗和利妥昔单抗3款产品为产品总收入贡献了决定性力量。
但贝伐珠单抗和利妥昔单抗为生物类似药,面临着激烈的市场竞争,据药智数据显示,2023年上半年,齐鲁制药和罗氏分别占贝伐珠单抗国内市场份额的53.63%和19.55%,信达生物仅占15.01%,同时还要面对盛迪亚生物、博安生物和百奥泰等7家药企的竞争;利妥昔单抗竞争药企虽然不多,但信达生物仅占国内市场份额的12.73%。
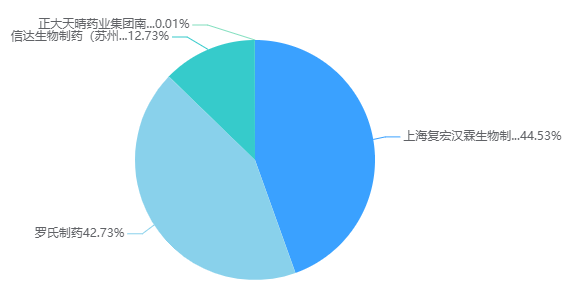
图3 国内利妥昔单抗市场份额占比情况
图片来源:药智数据
作为肿瘤业务的最重磅产品,信达生物不断拓展信迪利单抗适应症以及开辟内地以外市场。2023年5月,新增了用于EGFR-TKI治疗失败的EGFR基因突变阳性晚期或转移性非鳞状非小细胞肺癌的适应症;2024年2月,获中国澳门ISAF批准上市,但面临未来的PD-L/L1市场整体下滑,信达证券预测信迪利单抗在2027年实现最多45.55亿元的销售峰值,这离200亿目前还有一定差距。
寻求强项外的突破口。托莱西单抗的获批,成为信达生物产品格局的转折点,让其不再像过去一样停滞在肿瘤癌症领域,而信达生物撤回帕萨利司片的上市申请,还有一个目的就是将资源集中投入在更多重要管线上。
除了可能在国内独霸TED市场的IBI311外,玛仕度肽也将成为信达生物未来产品收入的最要支撑。据玛仕度肽中国肥胖受试者2期临床数据显示,给药48周后,9mg组体重降幅相较安慰剂组差值达−18.6%,比目前最火的司美格鲁肽和替尔泊肽的疗效更优异。
此外,玛仕度肽受试者能同时在腰围、血压、肝酶、甘油三酯、低密度脂蛋白胆固醇和血尿酸6项代谢指标上获益,9mg组治疗24周后,基线肝脏脂肪含量超5%受试者的肝脏脂肪含量较基线平均下降73.3%;所有受试者丙氨酸氨基转移酶(ALT)水平相对安慰剂组下降45.5%;甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)和血尿酸水平(UA)降幅也显著优于安慰剂。
玛仕度肽的同类潜在最佳疗效,加上IBI311独霸国内市场的潜能,信达生物200亿目标梦想将实现一半。
此外,信达生物还在采取“群狼”创新产品迭代计划,有超30个候选药物处于临床阶段,其中处于临床1/2期有多达20个。

图4 信达生物产品组合计划
图片来源:信达生物官微
据信达生物2023年H1报显示,截至2023年6月拥有现金及短期金融资产约15亿美元,加上已上市产品收入的持续“输血”,后续重磅产品临床研究也不愁资金来源。
04
结语
从Biotech到Biopharma,信达生物梦想成真,从肿瘤癌症领域向多个领域进军,也顺利实现,百亿级Biopharma的梦想,也将随着多个重磅产品的获批愿望成真。
2.《Horizon的Teprotumumab发现之旅:从罗氏肿瘤弃药到TED之光,首年8亿美元的罕见病新药》,凯莱英医药
来源:药智网 ,作者赵言午
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。

