合作十年,产品已上市,珐博进为何从诺奖级公司沦落为AZ“弃子”?
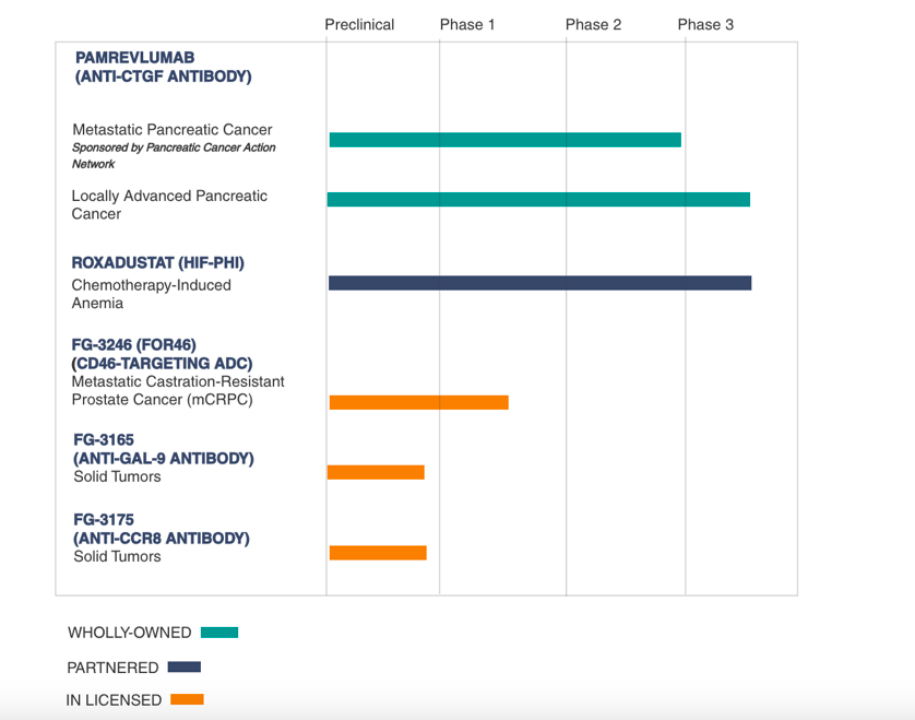
凭借对科学的坚持最终成功的制药公司不胜枚举,再生元、安进、福泰都是行业典范,但当执着变得盲目,只重科学,不重经营,或许最终还是难以觅得果实。近期,珐博进(Fibrogen)宣布,已经与AZ终止关于罗沙司他的合作,将收回罗沙司他在美国及其他地区的所有权利(除了中国和韩国)。如果时间回到2019年,这可能是珐博进最风光的一年。核心产品罗沙司他的作用机制获得诺贝尔生理学或医学奖;同年顶着“早于FDA,率先在中国获批”的光环上市,并获合作方AZ力推;在首部《中国肾性贫血诊疗临床实践指南》中斩获“最高推荐力度”。一时间风光无两,所有人都在看好罗沙司他,这颗头戴诺奖光环、率先诞生在中国的FIC新星,受到FDA的认可或许只是时间问题。然而短短不过四年时间,珐博进的高光只停留在了2019年。HIF-PHI类药物在FDA屡屡受挫,罗沙司他临床难获突破,“上岸”也就成了“天方夜谭”。珐博进更是历经灵魂人物离世,核心产品临床失败,经营困境无奈裁员32%。珐博进的命运也像它的股价和市值一样直线下滑,如今不到2美元的股价与不到2亿美元的市值,尚不及2014年的水平。如今再遭AZ“分手”,从诺奖级公司沦为老大哥“弃子”,究竟是什么原因,让珐博进在短短四年就跌下神坛?其实像是AZ这样的大公司选品逻辑也很清晰:创新的作用机制+可观的市场潜力。珐博进也是凭借这一优势在2013年斩获了与AZ的合作。与很多基于一个突破性创新技术成立的生物技术公司相同,珐博进在1993年创立也是对于“结缔组织生长因子(CTGF)和缺氧诱导因子(HIF)”的创新药开发。通常意义上,肾性贫血是慢性肾脏病(CKD)患者常见的临床并发症之一,发生率高达80%。临床上长期以促红细胞生成刺激剂(ESAs)等传统疗法进行治疗,但ESAs对于存储条件要求高,还需要辅以铁剂进行治疗,同时还可能会伴随心血管事件、肿瘤等安全性风险,并且其治疗有效性也并不高。而在20世纪90年代,科学家们发现了细胞可以通过感知氧气浓度对HIF进行调节,来应对机体氧含量的变化。彼时还是一名投资人的珐博进创始人Thomas Neff当时发现了这一研究的应用潜力,和科学家Kari Kivirikko共同创办了珐博进。在1999年,von Hippel−Lindau肿瘤抑制蛋白(pVHL)终于被证实在HIF-1a氧依赖蛋白水解中发挥关键作用,低氧能够诱导缺氧诱导因子刺激促红细胞生成素产生来促进红细胞的合成。而Thomas Neff创办的珐博进是当时行业中较早研发HIF-PHI类药物的公司,也成为了当红炸子鸡。有专家评价,肾性贫血领域30年未有新机制新靶点药物问世,罗沙司他改变的绝不只是数字,而是真正引领了肾性贫血治疗模式变革。珐博进也因此在2004、2006年斩获了与安斯泰来在日本、欧洲、独联体国家(CIS)、中东和南非地区共同开发罗沙司他的合作;在2013年,更是吸引到了阿斯利康以8.15亿美元的总交易额获得罗沙司他在美国、中国以及安斯泰来未授权地区的开发和商业化权益。与大型跨国公司的合作+革命级的产品让珐博进在2014年登陆纳斯达克市场时的市值就超过了15亿美金。之后随着2018年罗沙司他用于治疗正在接受透析治疗的患者CKD引起的贫血适应证在中国市场率先上市,2019年又扩大至非透析CKD患者。珐博进的市值一路飙升超过50亿美金。但好运并未一直伴随珐博进。虽然罗沙司他顶着光环进入了中国市场,但却迟迟敲不开美国市场的大门。最一开始其实FDA只是对罗沙司他治疗CKD贫血的安全性存疑,在2019年珐博进和阿斯利康联合公布了罗沙司他的安全性结果,但该结果被FDA认为其在心血管副作用上相较于传统的促红细胞生成素类药物阿法依泊汀,并未体现出优势,并对其上市评定日期一推再推。有意思的是,在推迟期间,珐博进还公开承认更改了部分用于分析罗沙司他在CKD患者的心脏安全性数据,其股价还因此大跌43%。尽管如此,在2021年8月,珐博进还是收到了FDA的最终判决:“目前暂时不会批准罗沙司他的上市申请,并要求珐博进在再次提交上市申请之前进行额外的临床研究。”珐博进在前方屡屡受到FDA拒绝,后方又遭遇了竞品的快速赶超。2023年2月,GSK同样机制的新药daprodustat在FDA获批上市,成为首款治疗CDK贫血成人患者的口服药物。不过FDA还是将其适应范围限定在了“接受过透析患者”。值得注意的是,在多方拉扯期间,FDA还拒绝了另一款HIF-PH抑制剂Vadadustat的上市申请,也是出于对其安全性风险的担忧。成功上市的竞品被限定范围,另一竞品也遭拒绝,更是让罗沙司他的美国梦遥遥无期。伴随罗沙司他梦碎美利坚,这起十年的合作也最终走向了破裂。就如同当初看中罗沙司他的潜力,AZ如今与珐博进的分手或许也是由于其迟迟未兑现的市场预期。两家公司的分手实属无奈,珐博进的境遇更是让人惋惜。多年对于罗沙司他的高投入背后,珐博进的境况只能用“成也罗沙司他,败也罗沙司他”来形容。首先在营收方面,成立于1993年的珐博进,发展至今其产品收入仍然不能覆盖运营和研发成本。珐博进在2021年到2023年的总营收分别为2.35亿美元、1.41亿美元和1.48亿美元,其中自2022年起,罗沙司他在中国市场的销售已经占据珐博进收入的一半以上,到2023年甚至已经占比达到68%。珐博进的研发支出在2021年到2023年却居高不下,分别为3.87亿美元、2.97亿美元和2.83亿美元。罗沙司他的销售显然并不能覆盖珐博进的运营与研发,甚至单研发投入就已经达到了其收入的近两倍,这让缺少美国市场的影响也更加显而易见。而在产品层面,从珐博进的官网来看,实际上仅有包括罗沙司他在内的三款临床产品,这其中还有一款ADC产品是引进而来。珐博进的财务状况更是让人担忧。据其2023年财报披露,截至2023年12月31日,公司现金和现金等价物为1.137亿美元,短期投资总额为2.663亿美元,长期投资为430万美元。当然,珐博进的自救措施也极为明显。2023年7月,珐博进披露了一项裁员计划,为降低运营成本,计划削减美国团队约32%,即104名员工。不过遗憾的是,伴随裁员计划,珐博进首席执行官Enrique Conterno还宣布了辞职。融资也成为珐博进在2022年以来最为频繁的动作:2022年11月,珐博进通过特权使用费融资的方式获得NovaQuest Capital的5000万美元融资;2023年5月,珐博进获得摩根士丹利1.5亿美金的非稀释性定期贷款。值得注意的是,珐博进在与摩根士丹利的合作公告中披露,1.5亿美元将大部分用于其治疗罕见病的管线Pamrevlumab的开发。而该产品也代表了继罗沙司他后,珐博进的一半想象空间。据悉,Pamrevlumab同罗沙司他一样,也是一款FIC潜力股,靶向CTGF,在特发性肺纤维化(IPF)、局部晚期不可切除胰腺癌(LAPC)和杜氏肌营养不良症(DMD)等多个罕见病领域被寄予厚望。其中,治疗IPF、DMD两项适应证上已经屡屡碰壁,治疗LAPC适应证的临床III期结果预计在今年上半年披露。珐博进的另一半想象空间则在罗沙司他的中国市场和目前仍在临床早期的ADC产品。罗沙司他虽然在美国市场“折戟”,在中国市场却十分受欢迎,这或许也是AZ选择保留中国市场权益的原因之一。珐博进2023年财报显示,截至2023年12月,罗沙司他是中国排名第一的CKD贫血产品,占据约42%的市场份额,并在血液透析、腹膜透析和非透析三个领域得到广泛采用。同时,其治疗化疗引起的贫血的新适应症申请已经递交CDE,有望成为因化疗引起的贫血的新型口服治疗选择。去年5月,珐博进还引进了一款CD46 ADC药物FG-3246,用于治疗转移性去势抵抗性前列腺癌 (mCRPC),目前处于临床I期。其实总结来看,Pamrevlumab在罕见病领域的应用是否随着临床开发碰壁而失败暂且无法下定论,罗沙司他在贫血上的应用未来或许也仍有转机,珐博进能够将两款FIC产品开发到如今的阶段也已经证明其实力,未来能否自救成功仍然需要时间来回答。https://xueqiu.com/9408056484/195334065
来源:E药经理人 ,作者CM10 公司E眼
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。