近日,北京市医疗保障局等9部门发布《北京市支持创新医药高质量发展若干措施(2024)(征求意见稿)》,“地域创新药新政”再次被推上风口浪尖,一份关于创新药新政的“特色菜单”,正在预制中。
01
创新药迎利好,
涉及北京百余家药企
新药研发是对时间和资金的双重考验,两者又互为影响,据前瞻产业研究院报告显示,创新药从研发到批准上市需经历9.5-15年,投入资金在23-27亿美元。
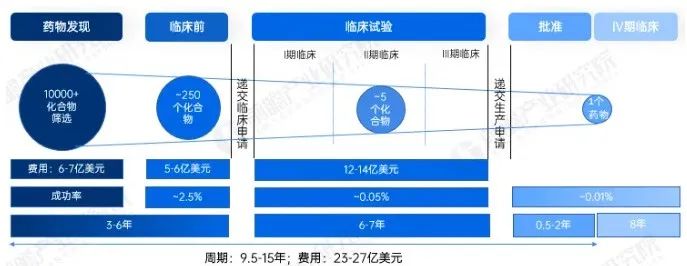
图1 创新药研发生产流程
图片来源:前瞻产业研究院
国内监管机构从2015年7月开始出台改革措施,缓解了创新药申请积压,同时鼓励创新药物开发,与改革前(2010年1月至2015年6月)相比,改革后(2015年7月至2020年12月)的IND审批时间缩短了414天,NDA审批时间缩短了441天,2018年7月开始,NMPA将药物临床试验审批程序调整为默示许可制度,但从整个临床试验阶段的长度而言,改革后和改革前的差异并不显著(2572天vs 2688天)。
如果说资金是压倒创新药研发“骆驼”的硬“压强”,那么,时间就是压倒“骆驼”的软“刀子”,时间周期的长短,在很大程度上决定着资金的多少,以及资金链的松紧。
《北京市支持创新医药高质量发展若干措施2024(征求意见稿)》对创新药最大的影响就是时间上的“照顾”,将临床试验启动整体用时压缩至28周以内,并持续加速;推动实施“药品补充申请审评时限从200日压缩至60日、药品临床试验审批时限从60日压缩至30日”的国家创新试点。
值得一提的是,将对创新药企实施重点项目制管理机制,在注册申报、许可办理等方面“一品一策”、提前介入、全程指导,“保姆”式的服务也将为创新药的研发扫清时间上的障碍。
此外,在支付端,将治疗费用较高的国谈药品纳入按固定比例支付,减轻参保人员费用负担;对符合条件的新药新技术费用,不计入DRG病组支付标准,单独支付;鼓励商业保险公司与医疗机构、医药企业合作,并建立“北京普惠健康保”特药清单动态调整机制,为创新药上市后的成本回收打通渠道。
据药智数据企业版——区域产业分析系统查询显示,北京地区主营业务为化药的企业有265家,中药企业有131家,生物制品企业有129家,原料药企业有14家,共计539家。北京的创新药(含改良新药)申请临床及批准临床数量在2019年以来就呈持续增长趋势,2023年分别达185个和149个。
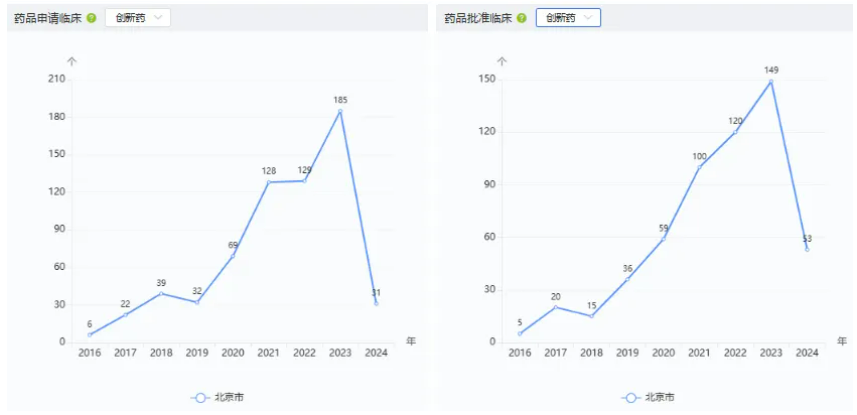
图2 2016年以来,北京创新药及改良新药临床情况
图片来源:药智数据
若征求意见稿顺利通过,北京又将迎来一波新药研发的高潮。
此外,在疾病领域方向,将有多个疾病领域的药品及药企占据“地利”因素,肿瘤领域最多。
作为肿瘤药物研发先锋,百济神州旗下产品泽布替尼2023年全球销售额达到近13亿美元,成为国产创新药首个“十亿美元分子”。此外,上述药企中,多数在肿瘤领域同样有创新药布局,如四环医药、神州细胞、中国医药、诺诚健华、华夏生生药业、祐和医药、加科思等,就连专注于糖尿病代谢领域的甘李药业,也布局的有肿瘤新药GLR2007。
值得一提的是,四环医药在肝病领域,神州细胞在罕见病、HPV疫苗和银屑病,中国医药在勃起功能障碍,诺诚健华在自免疾病领域,华夏生生药业在肝炎,舒泰神在汗腺炎、癌痛、哮喘和罕见病,都有创新药布局。
而作为与百济神州一样专注某个固定领域的甘李药业,在糖尿病代谢领域也将迎来空前的发展机遇。
历经磨难的CXO,部分企业终能扳回一局。近年来,受美国政策,以及韩国CXO抢单的影响,加上创新药的持续“寒冬”,CXO行业可谓是历经波折,在北京不乏康龙化成和阳光诺和等CXO药企。
北京创新医研发新政,将为CXO药企承接国外创新药进入中国市场的临床订单提供更大的便利,CXO资本市场信心也将逐步恢复。
02
管线产品丰富,
创新药研发哪家强?
百济神州进入临床阶段的自研产品管线中,有Sonrotoclax、欧司珀利单抗、BGB-A445、BGB-16673、BGB-21447等13款产品,其中,Somrotoclax和欧司珀利单抗已处于3期临床阶段。

图3 百济神州自研产品管线
图片来源:百济神州公告
Sonrotoclax是第二代BCL-2抑制剂,此前已获美国FDA授予治疗AML、MM、WM和MCL孤儿药认定,且有多项研究在2023年第65届美国血液学会(ASH)年会上展示。
据1/2期研究数据显示,初治(TN)CLL/SLL患者接受Sonrotoclax联合泽布替尼治疗,耐受性良好,且未出现肿瘤溶解综合征(TLS)病例,缓解率达到100%,无患者出现疾病进展(PFS)。
此外,Sonrotoclax单药治疗R/R边缘区淋巴瘤患者ORR为67%(n=8),其中4名患者(33%)达到完全缓解(CR);640mg组ORR为78%(n=7),其中4名患者(44%)达到CR;在先前接受BTK治疗时出现进展的所有4名患者中均观察到PR或更好缓解。
甘李药业的创新药管线产品虽然不多,只有GZR18(片)、GZR101、GZR4和GLR2007等4款,但每款产品对其今后的发展都有着极为重要的作用。
GZR101是甘李药业自主研发的新型预混双胰岛素复方制剂,由在研的长效基础胰岛素GZR33(50%)与速效门冬胰岛素(50%)混合制成,截至2023年12月,全球已上市的双胰岛素产品仅有诺和诺德的Ryzodeg;GZR4是第四代胰岛素,为每周皮下注射给药一次的超长效胰岛素周制剂,目前,全球范围内尚未有胰岛素周制剂产品被批准上市,进展最快的是诺和诺德的胰岛素周制剂Icodec,2024年3月,欧洲CHMP通过一项积极意见,建议批准Icodec用于治疗成人糖尿病。
甘李药业作为深耕糖尿病领域的药企,胰岛素产品对其业绩有着重要的支撑,营收主要来自胰岛素制剂及胰岛素干粉的销售收入,因此,胰岛素产品的更新升级对甘李药业来说,是其能否在糖尿病领域继续立足的根本。
神州细胞在创新药上的布局横跨罕见病、肿瘤、眼病及新冠等多个领域,包括2023半年报显示的SCT800、SCT200、SCT-I10A、SCT1000、SCT510A、SCTV01、SCT650C,以及近期获批临床的SCTC21C和SCTB35。
图4 神州细胞在研项目
图片来源:神州细胞2023半年报
SCT800是治疗罕见病甲型血友病的首个国产重组八因子产品,也是神州细胞的首款上市产品,于2021年7月获批上市,据2022年报显示,首个完整年度销售收入为10.23亿元,而神州细胞当年收入全部来源于此。据2023年报显示,该产品销售额继续大幅增长,销售额约17.8亿元,同比增长超77%,且神州细胞营收依然主要来自于该药,营收同比增长84.46%,达18.87亿元。
在神州细胞的创新药管线上,还有一款潜在的超爆款产品SCT1000,为全球首个进入临床的14价HPV疫苗,目前已处于3期临床试验阶段。虽然国产HPV疫苗早已上市,但面对进口9价HPV疫苗在解决供应端不足及年龄扩展后的的强势,高价HPV疫苗依然受到接种者追捧,神州细胞的SCT1000也被誉为最有实力打破进口高价HPV疫苗的选手之一。
北京地区药企的创新药亮点颇多,在这里就不一一列举。
03
结语
在2024年政府工作报告中,创新药首次被提及,充分表明了国家对创新药的决心及信心,随着北京等地创新药新政的推进,全国范围各具特色的创新药新政“菜单”即将来袭。
3.前沿产业研究院《2023年中国创新药行业全景图谱》
来源:药智网 ,作者赵言午
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。

