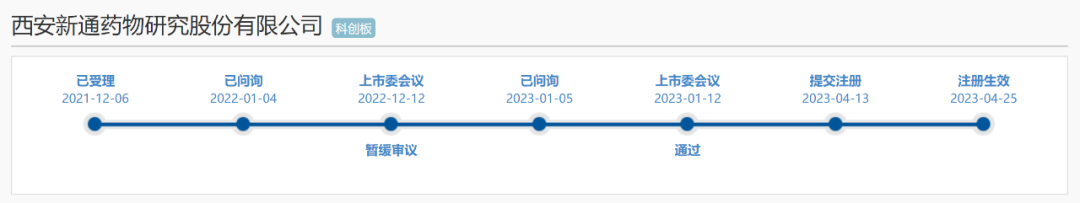
4月25日,对于西安新通药物研究股份有限公司(简称:新通药物),是一个特殊的日子。
2023年4月25日,新通药物获得中国证监会的批复,同意其科创板首次公开发行股票的注册申请。按照现行法规,上述批复中也明确指出:本批复自同意注册起12个月内有效。
根据此前科创板上市企业的平均数据,上市企业从拿到证监会的注册批文,到新股成功发行,平均用时是41天,所以理论上,12个月的有效期是一个极其宽裕的时间期限。但是,从2023年4月25日,到2024年4月25日,整整一年已经过去,新通药物仍然没有完成新股发行。
这意味着,科创板历史上,第一家拿到IPO注册批文后,在新股发行阶段失败的药企,正式诞生了!位于西安的新通药物,成立时间超过20年,最初以化学药仿制、中药研发起步,后续逐渐转型为创新药研发企业,目前主要聚焦于乙肝、肝癌等疾病领域。客观地说,新通药物此前的IPO之路也不是特别顺利。2021年12月6日,新通药物按照“标准五”提交IPO申请材料,在12个月之后的2022年12月12日,经历了上会前的“暂缓审议”。一般在上会之前出现“暂缓审议”,肯定是很不好的苗头,但是暂缓审议也并非意味着企业的上市之路就此折戟,只要发行人、中介机构能后续将相关事项核查披露清楚,按照规则还能再度上会。果然,此后新通药物的表现非常给力,在1个月的时间内完成了问询与回复的过程,并且在2023年1月12日顺利过会。3个多月以后,新通药物拿到证监会的IPO注册批文,可以说距离最终的胜利已经只有吹弹可破的最后一厘米的距离。
但是非常不幸,新通药物的IPO大业,还是倒在了这最后一厘米。截至2023年4月,新通药物一共披露了9款在研管线,其中4款还处于临床前的初级研发状态。
在已经进入临床试验的5款药物中,仅有1款处于1期临床试验的HBV 核衣壳蛋白装配抑制剂自主研发,其余4款为都是授权引进或者合作开发的管线。
在答复审核委员会的问询函中,新通药物强调了自身对于引进的化合物和专利技术的原创性工作。
比如,新通药物强调独立完成了甲磺酸帕拉德福韦片的临床前研究,发现最佳给药剂量,并选择一线对照药物完成I期/II期/III期临床试验;
比如,新通药物独立重新完成了注射用MB07133产品临床前研究,开发了新剂型,目前已重新完成I期/II期第一阶段临床试验,并拓展与信迪利单抗联合用药治疗晚期原发性肝癌的一线疗法。
以上这些工作,固然也属于研发的范畴,对于管线的发展也起了推动作用,但是能否体现硬核的“科创属性”,就是一个见仁见智的问题了。
事实上,新通药物的研发投入并不高,从2020年到2022年,三年研发费用分别为9254万元、6313万元、5485万元。
同时,其研发工作高度依赖外部CRO。
招股说明书显示,新通药物与多家外部企业签订了临床研究委托协议以及合作研发协议,从2020年到2022年,外包采购金额占研发投入的比重分别为74%、60%、59%。
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。