2024年可以说是细胞和基因治疗(CGT,Cellular and Gene Therapy)爆发的一年。
2月,全球首款TIL疗法在美国获批上市,其用于治疗PD-1抗体治疗后进展的晚期黑色素瘤,打响了细胞治疗实体瘤的全球首枪。4月,美国FDA批准辉瑞的AAV基因疗法BEQVEZ(fidanacogene elaparvovec-DZKT)上市,用于治疗中度至重度血友病B且对AAV血清型Rh74的中和抗体检测为阴性的成年(18岁及以上)患者。
在中国,CGT行业发展也如火如荼,尤其是在细胞治疗行业已与美国形成并驾齐驱之势。4月,传奇生物的CAR-T疗法Carvykti在欧盟获批用于二线治疗复发性或难治性多发性骨髓瘤(RRMM)成人患者。另外,4月有8款细胞疗法首次在国内获批临床,包括肿瘤浸润淋巴细胞(TIL)疗法、干细胞药物、γδ T细胞药物、CAR-T细胞药物、TCR-T细胞药物、CAR-raNK细胞疗法等多种形式。
近日,在CBIITA联合体、药智网主办的一场线上会议上,重庆医科大学药学院教授、博士生导师冯涛,中源协和副总经理兼首席科学官、中源药业CEO、CBIITA联合体干细胞再生医学专委会主委张宇,及主持人康洲医药大数据研究院副院长刘中卫博士共同探讨了CGT行业的挑战、机遇与前景。
中美两国领跑细胞治疗赛道
“在整个生物医药领域,细胞疗法是为数不多的我国能够与美国并驾齐驱的赛道。”张宇说到。
药智数据显示,全球细胞疗法研发集群分别为北美(主要是美国)、东亚(包括澳大利亚)以及西欧(包括以色列)。美国和中国在国际细胞疗法的研发中占据主导地位,适应症主要集中在肿瘤领域,逐步向非肿瘤领域扩展。
目前,美国有6款CAR-T药物上市,其中Carvykti原研为南京传奇生物。我国也已有5款CAR-T药物上市,靶点都包含CD19、BCMA靶点。
表1. 中美上市CAR-T产品对比
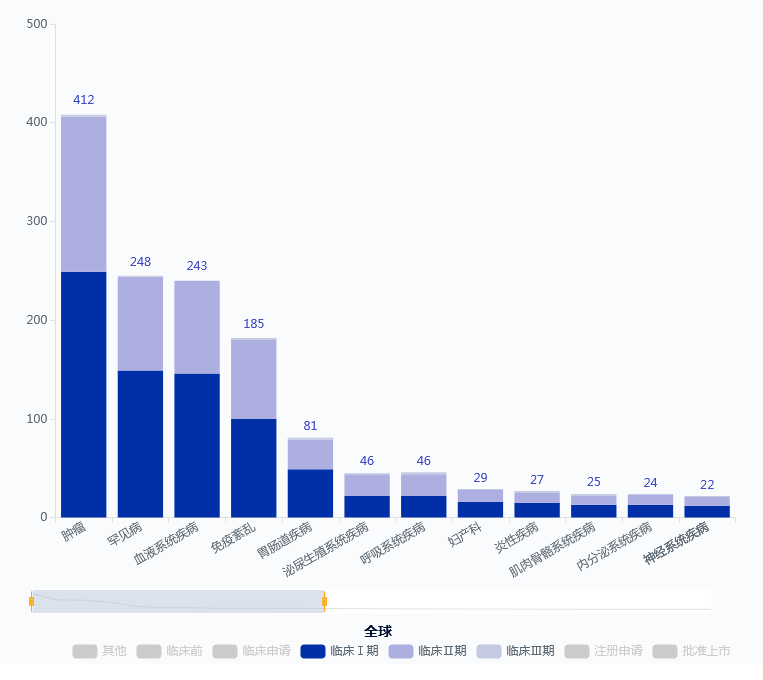
数据来源:药智数据 此外还有400多款国产细胞疗法已进入临床研究阶段,适应症涵盖肿瘤、罕见病、血液系统疾病等治疗领域。 临床阶段的国产细胞疗法适应症分布情况 图片来源:药智数据 细胞疗法由血液瘤向实体瘤迈进 从适应症来看,目前CAR-T疗法适应症都是血液瘤。 为什么细胞疗法率先在血液瘤取得突破,而不是实体瘤?张宇认为,血液肿瘤人群虽然在整个肿瘤领域占比不到10%,但它相对来说比较好治。因为大多数抗肿瘤药都是静脉给药,药物一旦进入血液就可以与肿瘤细胞无障碍接触,产生杀伤、治疗效果。但是实体肿瘤,不是一群散兵游勇,更像是有组织的黑社会,所以想要干掉它,相对来说不会那么容易,需要在技术研究和转化研究方面做更多努力来升级、增强平台功能,才能达到治疗效果。 目前上市的血液瘤细胞疗法大都属于二代CAR-T,想要治疗实体瘤有一定困难。但是现在一些新类型细胞疗法已在实体瘤领域取得了突破性进展。 2024年2月,美国FDA加速批准Iovance Biotherapeutics公司的肿瘤浸润淋巴细胞(TIL)疗法Amtagvi(lifileucel),用于治疗晚期黑色素瘤。根据Iovance新闻稿,Amtagvi是第一款获批的TIL疗法,也是首款获批治疗实体瘤的T细胞疗。TIL与CAR-T、TCR-T不同之处在于,TILs是从患者自身的肿瘤样本中采集浸润的淋巴细胞,之后在体外进行扩增培养,最后再回输到患者体内。TILs细胞相当于适应性免疫系统的前线士兵,具有低脱靶毒性及优越的肿瘤病灶浸润能力,可被招募到肿瘤部位直接对抗肿瘤,在治疗实体瘤方面具有独特的优势。 今年8月,Adaptimmune公司靶向MAGE-A4的TCR-T细胞疗法Afami-cel有望获得美国FDA批准用于治疗晚期滑膜肉瘤。如若获得批准,将成为全球首款获批的TCR-T细胞疗法以及首款获批的实体瘤T细胞疗法。 随着技术的不断更新、成熟,细胞疗法有望从10%的血液瘤市场迈向90%的实体瘤市场。 在中国,目前也有多家企业布局实体瘤细胞疗法,包括沙砾生物、华赛伯曼、君赛生物、西比曼生物、原启生物等,有望与美国形成并驾齐驱之势。 展望未来:挑战与机遇并存 尽管市场前景广阔,但CGT企业还需要克服安全性、工业化生产、物流、支付、使用等多项医药行业面临的共性和个性问题。 在生产方面,细胞疗法属于精准医疗,与小分子和抗体药物相比在生产模式上有很大区别,每批产品仅可供一人使用,产量无法实现指数级放大。而且细胞产品是一种活的药物,在出境等方面也面临很大挑战。原本单一工厂可以满足全球患者的需求,但细胞疗法可能需要在不同地区建立多个工厂以满足产能需求。尽管通用型产品的开发可能从技术上解决这一问题,但这仍需时间来实现。 另外,物流也有挑战,细胞疗法的有效期往往按天计算,如何保证细胞产品能够如期、准确送达医院供患者使用,需要企业有系统的管理方案。 最后,细胞疗法,特别是自体细胞疗法,需要采集患者细胞或组织,再进行加工,最后回输到患者体内。与传统用药相比,这一套流程增加了患者与药企的接触机会,更像是一种一对一的服务,所以企业除了要考虑生产、运输,还有做好患者服务。 在商业化方面,美国得益于商业保险的支持,细胞疗法商业化取得不错成绩。但是在国内,细胞疗法百万的治疗费用让很多患者却步。一方面,我们需要完善多平台保障体系;另一方面,还需要一些慈善计划;同时企业也要努力降低成本,惠及更多患者。 近日,印度推出低价CAR-T产品引发产业界广泛讨论。张宇认为,我国在现有的100万基础上,CAR-T价格有一定下降空间,但要降到更低的二十万水平还需要靠技术的迭代升级,或者开发新的治疗方法。 展望未来,专家们提出了几个关键点: CGT是中国生物医药领域中最年轻且与国际接轨最近的赛道,目前处于与美国并跑态势。 在并跑的基础上想要实现领跑,最重要的是原始创新,不能仅依赖模仿他人技术,要拥有自主的知识产权。 另外,我们需要全面认识疾病,而不仅仅关注技术本身,这将有助于更有效地应用CGT技术。在转化研究方面,也需要在监管和临床角度进行更多工作。 最后,监管不应盲目崇拜FDA的批准,而应基于科学证据进行决策。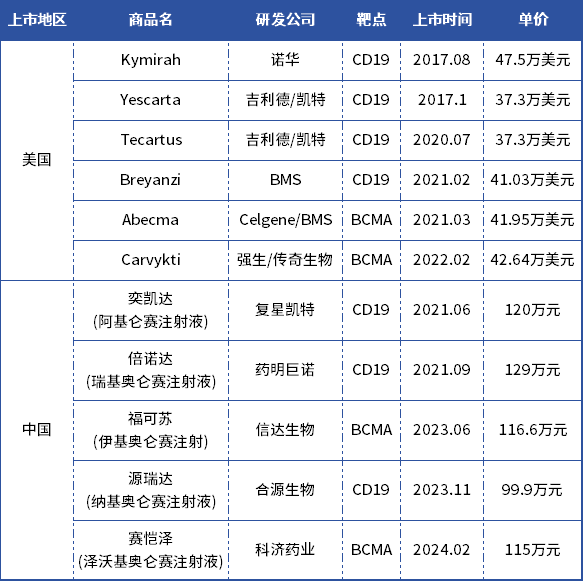
来源:药智头条 ,作者游游
声明:本文观点仅代表作者本人,不代表煜森资本立场,欢迎在留言区交流补充。如需转载,请注明文章作者和来源。如涉及作品内容、版权和其它问题,请在本平台留言。

